Acido selenico
| Acido selenico | |
|---|---|
 | |
 | |
| Nome IUPAC | |
| acido tetraossoselenico(VI) | |
| Nomi alternativi | |
| acido selenico | |
| Caratteristiche generali | |
| Formula bruta o molecolare | H2SeO4 |
| Massa molecolare (u) | 144,97 |
| Aspetto | solido incolore deliquescente |
| Numero CAS | |
| Numero EINECS | 2319794 |
| PubChem | 1089 e 21713352 |
| DrugBank | DBDB11068 |
| SMILES | O[Se](=O)(=O)O |
| Proprietà chimico-fisiche | |
| Densità (g/cm3, in c.s.) | 2,95 g/cm³ |
| Indice di rifrazione | 1,5174 |
| Costante di dissociazione acida a 298 K | Ka1 >> 1 Ka2 = 1,2·10−2 |
| Temperatura di fusione | 58 °C (331 K) |
| Indicazioni di sicurezza | |
| TLV (ppm) | non assegnato |
| Simboli di rischio chimico | |
  
| |
| Frasi H | 301 - 331 - 373 - 410 |
| Consigli P | 261 - 273 - 301+310 - 311 - 501 [1][2] |
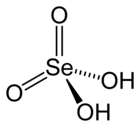
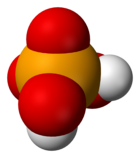
L'acido selenico è l'ossoacido del selenio esavalente, avente formula molecolare H2SeO4 o, in forma semistrutturale, (O=)2Se(OH)2. La molecola è tetraedrica con l'atomo di selenio al centro (Se ibrido sp3),[3] analoga e isoelettronica di valenza a quella dell'acido solforico H2SO4, con il quale l'acido selenico ha in comune molte proprietà mentre, a parte valenza e stato di ossidazione, risulta essere parecchio diverso dall'acido tellurico già a partire dalla formula molecolare: H6TeO6 o Te(OH)6.[4]
Proprietà e struttura
[modifica | modifica wikitesto]L'acido selenico si presenta a temperatura ambiente in forma di cristalli incolori fortemente igroscopici e deliquescenti,[5] aghiformi o prismatici, solubilissimi in acqua, che a 58 °C fondono in un liquido viscoso incolore.[6] Come il solforico, l'acido selenico è un acido biprotico forte in prima dissociazione e debole in seconda;[7] tuttavia, in quest'ultima si mostra leggermente più forte del solforico: pKa2(H2SeO4) = 1,7, contro 1,99 di H2SO4.[8] Come l'acido solforico, è fortemente disidratante (anche in soluzione concentrata) e può carbonizzare molte sostanze organiche; forma diversi idrati, in particolare, H2SeO4 · H2O (p. f. 26 °C) e H2SeO4 · 4 H2O (p. f. 52 °C).[9] I suoi sali sono spesso isomorfi ai solfati, ricalcandone anche le solubilità in acqua;[10] in particolare il selenato di bario (BaSeO4) e quello di piombo (PbSeO4) risultano praticamente insolubili in acqua. Inoltre, l'acido selenico si combina facilmente con la sua anidride (SeO3) dando l'acido piroselenico (H2Se2O7) in cui un ossigeno a ponte collega due gruppi −SeO3H, del tutto analogo al pirosolforico (H2S2O7). In analogia al'acido perossimonosolforico (acido di Caro, H2SO5), esiste l'acido monoperossiselenico H2SeO5.[9]
L'acido selenico si differenzia notevolmente dall'acido solforico, invece, in quanto ha proprietà decisamente ossidanti.[7] Questo comportamento riguarda il selenio esavalente ed è una caratteristica comune ad altri elementi del 4 ° periodo che vengono dopo la prima serie di transizione nelle loro valenze massime, in particolare As(V), Se(VI) e Br(VII); la condizione di tali elementi è nota con l'espressione «riluttanza ad assumere la massima valenza» ed è in linea anche con il concetto affine di coppia inerte che si osserva per i sottostanti elementi del 6° periodo che vengono appena dopo la terza serie di transizione.[11][12]
Struttura
[modifica | modifica wikitesto]Nella molecola dell'acido selenico il selenio è al centro di un tetraedro distorto ai cui vertici sono posti due ossigeni, legati con doppio legame e due ossidrili, con legami semplici. La distanza Se−O nel selenato di potassio K2SeO4, in quanto specie rappresentativa per lo ione selenato, è di 164,8 pm;[13] come atteso per il maggior raggio covalente del selenio rispetto allo zolfo, questa distanza è un po' maggiore della distanza S−O nell'analogo solfato di potassio (K2SO4), che ammonta a 147 pm.[14]
Sintesi e reattività
[modifica | modifica wikitesto]A differenza che nel caso dell'acido solforico, il metodo di preparazione dell'acido per reazione diretta dell'anidride con l'acqua non risulta pratico per l'acido selenico.[15] Può essere preparato per azione di ossidanti forti su selenio, diossido di selenio, o acido selenioso:
L'ossidazione dell'acido selenioso può anche essere effettuata con fluoro, acido clorico o ozono; l'ossidazione con cloro non è completa ed è reversibile. Un'altra via consiste nell'ossidazione elettrolitica dell'acido selenioso e in tal modo la reazione può essere completa.[16]
L'acido selenico partecipa dell'instabilità generale dei composti del selenio esavalente: per riscaldamento intorno a 200 °C inizia a decomporsi in acido selenioso rilasciando ossigeno:[17]
2 H2SeO4 → 2 H2SeO3 + O2 ↑
Poi, verso i 260 °C la reazione diviene più rapida e l'acido selenioso prodotto si disidrata a SeO2.[9] Per confronto, l'analoga reazione per l'acido solforico, più stabile, avviene intorno al raggiungimento del suo punto di ebollizione, a circa 300 °C.[18]
Inoltre, ha spiccate proprietà ossidanti: E°(HSeO4− / HSeO3−) = 1,15 V in ambiente acido, riuscendo ad ossidare reversibilmente lo ione cloruro a cloro elementare:
In presenza di quantità anche molto piccole di cloruro, che funge da catalizzatore, l'acido selenico riesce ad attaccare l'oro ossidandolo a ione auroso [E°(AuCl2− / Au) =1,154 V]:[19]
In assenza di cloruri, ma a caldo, almeno a 230 °C, attacca l'oro dando soluzioni di selenato aurico [Au(III)]:[20]
2 Au + 6 H2SeO4 → Au2(SeO4)3 + 3 H2SeO3 + 3 H2O
In assenza di complessanti l'ossidazione dell'oro elementare ad Au(III) è più facile di quella ad Au(I): E°(Au(III) / Au) =1,52 V, E°(Au(I) / Au) =1,83 V.[21]
Tuttavia, in queste ed altre reazioni di ossidazione l'acido selenico non è cineticamente veloce.[10]
L'acido selenico reagisce con il fluoruro di selenoile per dare l'acido fluoroselenico, facilmente idrolizzabile, che è del tutto analogo all'acido fluorosolforico HSO3F (che invece si idrolizza con difficoltà):[22]
H2SeO4 + SeO2F2 → 2 HSO3F
Note
[modifica | modifica wikitesto]- ^ Sigma Aldrich; rev. del 19.03.2012, riferito alla soluzione acquosa al 40%
- ^ Smaltire presso un impianto di trattamento dei rifiuti autorizzato.
- ^ (EN) Satya Prakash, G. D. Tuli, S. K. Basu e R. D. Madan, 29, in Advanced Inorganic Chemistry, vol. 1, New Delhi, S. Chand & Company Pvt. Ltd., 2014, p. 477, ISBN 81-219-0263-0.
- ^ F. Albert Cotton, Geoffrey Wilkinson, Carlos A. Murillo e Manfred Bochmann, Advanced Inorganic Chemistry, 6ª ed., Wiley Interscience, 1999, p. 531, ISBN 0-471-19957-5.
- ^ (EN) PubChem, Selenic acid, su pubchem.ncbi.nlm.nih.gov. URL consultato il 16 dicembre 2023.
- ^ (DE) Georg Brauer, Handbuch der Präparativen Anorganischen Chemie, Vol. 1, 3ª ed., Stuttgart, Ferdinand Enke Verlag, 1975, p. 425, ISBN 3-432-02328-6.
- ^ a b N. N. Greenwood e A. Earnshaw, Chemistry of the Elements, 2ª ed., Butterworth-Heinemann, 1997, pp. 781-782, ISBN 0-7506-3365-4.
- ^ William M. Haynes, David R. Lide e Thomas J. Bruno, Dissociation Constants of Inorganic Acids and Bases, in CRC handbook of chemistry and physics : a ready-reference book of chemical and physical data., 2016-2017, 97th edition, ISBN 9781498754293, OCLC 957751024. URL consultato il 19 novembre 2018.
- ^ a b c (DE) Nils Wiberg, Egon Wiberg e Arnold Frederik Holleman, XIII. Die Gruppe der Chalkogene, in Anorganische Chemie, 103. Auflage, De Gruyter, 2017, pp. 721-723, ISBN 978-3-11-026932-1.
- ^ a b F.A. Cotton e G. Wilkinson, ADVANCED INORGANIC CHEMISTRY, Fifth Edition, Wiley Interscience, 1988, p. 526, ISBN 0-471-84997-9.
- ^ J. E. Huheey, E. A. Keiter e R. L. Keiter, Chimica Inorganica, Principi, Strutture, Reattività, 2ª ed., Piccin, 1999, pp. 913-921, ISBN 88-299-1470-3.
- ^ (DE) Arnold F. Holleman, E. Wiberg e N. Wiberg, IX. Hauptgruppenelemente, in Anorganische Chemie, 103ª ed., DE GRUYTER, 2017, pp. 332-333, ISBN 978-3-11-026932-1.
- ^ A. Kálmán, J. S. Stephens e D. W. J. Cruickshank, The crystal structure of K 2 SeO 4, in Acta Crystallographica Section B Structural Crystallography and Crystal Chemistry, vol. 26, n. 10, 1º ottobre 1970, pp. 1451–1454, DOI:10.1107/S0567740870004314. URL consultato l'8 giugno 2022.
- ^ K. Ojima, Y. Nishihata e A. Sawada, Structure of potassium sulfate at temperatures from 296 K down to 15 K, in Acta Crystallographica Section B Structural Science, vol. 51, n. 3, 1º giugno 1995, pp. 287–293, DOI:10.1107/S0108768194013327. URL consultato l'8 giugno 2022.
- ^ Don M. Yost e Horace Russell, Systematic inorganic chemistry: of the fifth-and-sixth-group nonmetallic elements, Nachdr., Prentice-Hall, 2009, ISBN 978-1-4067-7302-6.
- ^ (EN) Kirk-Othmer Encyclopedia of Chemical Technology, 1ª ed., Wiley, 26 gennaio 2001, DOI:10.1002/0471238961, ISBN 978-0-471-48494-3. URL consultato il 16 dicembre 2023.
- ^ Anil Kumar De, A Text Book of Inorganic Chemistry, New Age International, 2003, pp. 543-545, ISBN 81-224-1384-6.
- ^ N. N. Greenwood e A. Earnshaw, Chemistry of the Elements, 2ª ed., Butterworth-Heinemann, 1997, p. 707, ISBN 0-7506-3365-4.
- ^ Encyclopedia of electrochemistry. 7a: Inorganic electrochemistry / vol. ed. by Fritz Scholz, 7a, Wiley-VCH, 2006, p. 46, ISBN 978-3-527-30399-1.
- ^ (EN) Victor Lenher, ACTION OF SELENIC ACID ON GOLD. 1, in Journal of the American Chemical Society, vol. 24, n. 4, 1902-04, pp. 354–355, DOI:10.1021/ja02018a005. URL consultato il 16 dicembre 2023.
- ^ Standard potentials in aqueous solution, collana Monographs in electroanalytical chemistry and electrochemistry, Dekker, 1985, ISBN 978-0-8247-7291-8.
- ^ Robert Bruce King, Selenium: Inorganic Chemistry, in Encyclopedia of inorganic chemistry, 2nd ed, J. Wiley & sons, 2005, ISBN 978-0-470-86078-6.
Bibliografia
[modifica | modifica wikitesto]- I. Bertini, F. Mani, Chimica inorganica, CEDAM, ISBN 88-13-16199-9
- https://web.archive.org/web/20091024062252/http://www.ing.unitn.it/~colombo/selenio/chimica.htm
Voci correlate
[modifica | modifica wikitesto]Altri progetti
[modifica | modifica wikitesto] Wikimedia Commons contiene immagini o altri file su acido selenico
Wikimedia Commons contiene immagini o altri file su acido selenico





