Berylliumhydroxid
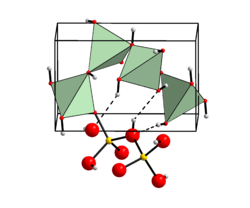
| Kristallstruktur | ||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| ||||||||||||||||
| _ Be2+ _ O2− _ H+ | ||||||||||||||||
| Allgemeines | ||||||||||||||||
| Name | Berylliumhydroxid | |||||||||||||||
| Andere Namen |
Berylliumdihydroxid | |||||||||||||||
| Verhältnisformel | Be(OH)2 | |||||||||||||||
| Kurzbeschreibung |
farbloses Gel[1] | |||||||||||||||
| Externe Identifikatoren/Datenbanken | ||||||||||||||||
| ||||||||||||||||
| Eigenschaften | ||||||||||||||||
| Molare Masse | 43,03 g·mol−1 | |||||||||||||||
| Aggregatzustand |
fest[1] | |||||||||||||||
| Dichte |
1,924 g·cm−3[2] | |||||||||||||||
| Löslichkeit |
kaum löslich in Wasser[3] | |||||||||||||||
| Sicherheitshinweise | ||||||||||||||||
| ||||||||||||||||
| Thermodynamische Eigenschaften | ||||||||||||||||
| ΔHf0 |
−902,5 kJ·mol−1[6] | |||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen (0 °C, 1000 hPa). | ||||||||||||||||
Berylliumhydroxid ist eine chemische Verbindung aus der Gruppe der Hydroxide.
Vorkommen
[Bearbeiten | Quelltext bearbeiten]In der Natur kommt Berylliumhydroxid in Form der seltenen bis sehr seltenen Minerale Behoit[7][8] und Klinobehoit[9][10] vor.
Gewinnung und Darstellung
[Bearbeiten | Quelltext bearbeiten]Berylliumhydroxid kann durch Ausfällen aus einer Berylliumsalzlösung durch Zugabe von Ammoniaklösung oder einer Lösung eines Metallhydroxides gewonnen werden.[3]
Besser gelingt die Darstellung von kristallinem Berylliumhydroxid jedoch aus einer heiß gesättigten Lösung von amorphen Be(OH)2 in einer 10 n NaOH-Lösung, über den Zwischenschritt der Bildung von Natriumtetrahydroxoberyllat und einer anschließenden langsamen Abkühlung.[11]
Eigenschaften
[Bearbeiten | Quelltext bearbeiten]Berylliumhydroxid ist ein farbloses Gel, das in Wasser praktisch unlöslich ist.[3] Beim Erhitzen über 400 °C zersetzt es sich zu Berylliumoxid:[3]
Es tritt in zwei Modifikationen α- und β-Berylliumhydroxid auf. Die Verbindung ist in frisch gefälltem Zustand amphoter, löst sich also sowohl in Säuren unter Bildung von [Be(H2O)4]2+, als auch in alkalischen Lösungen unter Bildung von [Be(OH)4]2−. Beim Kochen mit Wasser, beim Trocknen oder beim längeren Stehenlassen "altert" die Verbindung und wird schwerlöslich.[12][3] Es ist das einzige amphotere Hydroxid der Erdalkalimetalle.[13]
In der orthorhombischen Kristallstruktur von Berylliumhydroxid ist jedes Berylliumion von vier Hydroxidionen koordiniert, die ein nur geringfügig verzerrtes Tetraeder bilden. Da jedes Hydroxidion an zwei Be2+-Ionen gebunden ist, entsteht ein dreidimensionales Netzwerk eckenverknüpfter Tetraeder. Zwischen den Hydroxidionen bestehen zahlreiche Wasserstoffbrückenbindungen.[14]
Einzelnachweise
[Bearbeiten | Quelltext bearbeiten]- ↑ a b Eintrag zu Beryllium-Verbindungen. In: Römpp Online. Georg Thieme Verlag, abgerufen am 3. März 2012.
- ↑ Roger Blachnik (Hrsg.): Taschenbuch für Chemiker und Physiker. Begründet von Jean d’Ans, Ellen Lax. 4., neubearbeitete und revidierte Auflage. Band 3: Elemente, anorganische Verbindungen und Materialien, Minerale. Springer, Berlin 1998, ISBN 3-540-60035-3, S. 334 (eingeschränkte Vorschau in der Google-Buchsuche).
- ↑ a b c d e Egon Wiberg, Arnold Frederick Holleman: Inorganic Chemistry, Elsevier, 2001, ISBN 0-12352651-5.
- ↑ Eintrag zu Berylliumverbindungen in der GESTIS-Stoffdatenbank des IFA, abgerufen am 23. August 2021. (JavaScript erforderlich)
- ↑ Nicht explizit in Verordnung (EG) Nr. 1272/2008 (CLP) gelistet, fällt aber mit der angegebenen Kennzeichnung unter den Gruppeneintrag Berylliumverbindungen, ausgenommen Beryllium-Tonerdesilikate, und ausgenommen die namentlich in diesem Anhang bezeichneten im Classification and Labelling Inventory der Europäischen Chemikalienagentur (ECHA), abgerufen am 23. August 2021. Hersteller bzw. Inverkehrbringer können die harmonisierte Einstufung und Kennzeichnung erweitern.
- ↑ David R. Lide (Hrsg.): CRC Handbook of Chemistry and Physics. 90. Auflage. (Internet-Version: 2010), CRC Press / Taylor and Francis, Boca Raton FL, Standard Thermodynamic Properties of Chemical Substances, S. 5-6.
- ↑ Mineralienatlas:Behoit.
- ↑ Behoite. In: John W. Anthony, Richard A. Bideaux, Kenneth W. Bladh, Monte C. Nichols (Hrsg.): Handbook of Mineralogy, Mineralogical Society of America. 2001 (handbookofmineralogy.org [PDF; 69 kB; abgerufen am 22. November 2017]).
- ↑ Mineralienatlas:Klinobehoit.
- ↑ Clinobehoite. In: John W. Anthony, Richard A. Bideaux, Kenneth W. Bladh, Monte C. Nichols (Hrsg.): Handbook of Mineralogy, Mineralogical Society of America. 2001 (handbookofmineralogy.org [PDF; 69 kB; abgerufen am 22. November 2017]).
- ↑ Georg Brauer (Hrsg.), unter Mitarbeit von Marianne Baudler u. a.: Handbuch der Präparativen Anorganischen Chemie. 3., umgearbeitete Auflage. Band II, Ferdinand Enke, Stuttgart 1978, ISBN 3-432-87813-3, S. 893.
- ↑ A. F. Holleman, E. Wiberg, N. Wiberg: Lehrbuch der Anorganischen Chemie. 101. Auflage. Walter de Gruyter, Berlin 1995, ISBN 3-11-012641-9, S. 1106.
- ↑ Charles E. Mortimer, Ulrich Müller, Johannes Beck: Chemie: Das Basiswissen der Chemie. Georg Thieme Verlag, Stuttgart 2014, ISBN 3-13-171331-3, S. 473 (eingeschränkte Vorschau in der Google-Buchsuche).
- ↑ R. Stahl, C. Jung, H. D. Lutz, W. Kockelmann H. Jacobs: Kristallstrukturen und Wasserstoffbrückenbindungen bei β-Be(OH)2 und ε-Zn(OH)2. In: Zeitschrift für Anorganische und Allgemeine Chemie. 624, 1998, S. 1130.




