Azotna kiselina
| Azotna kiselina | |||
|---|---|---|---|
| |||
 |
 | ||
| IUPAC ime |
| ||
| Identifikacija | |||
| CAS registarski broj | 7697-37-2 | ||
| PubChem[1][2] | 944 | ||
| ChemSpider[3] | 919 | ||
| UNII | 411VRN1TV4 | ||
| EINECS broj | |||
| UN broj | 2031 | ||
| KEGG[4] | |||
| MeSH | |||
| ChEBI | 48107 | ||
| ChEMBL[5] | CHEMBL1352 | ||
| RTECS registarski broj toksičnosti | QU5775000 | ||
| Gmelin Referenca | 1576 | ||
| 3DMet | B00068 | ||
| Jmol-3D slike | Slika 1 Slika 2 | ||
| |||
| |||
| Svojstva | |||
| Molekulska formula | HNO3 | ||
| Molarna masa | 63.01 g mol−1 | ||
| Agregatno stanje | bezbojna tečnost | ||
| Gustina | 1,5129 g cm−3 | ||
| Tačka topljenja |
-42 °C, 231 K, -44 °F | ||
| Tačka ključanja |
83 °C, 356 K, 181 °F (68% rastvor ključa na 121 °C) | ||
| Rastvorljivost u vodi | Potpuno se meša | ||
| pKa | -1,4[6] | ||
| Indeks prelamanja (nD) | 1,397 (16,5 °C) | ||
| Dipolni moment | 2,17 ± 0,02 D | ||
| Termohemija | |||
| Standardna entalpija stvaranja jedinjenja ΔfH |
−207 kJ·mol−1[7] | ||
| Standardna molarna entropija S |
146 J·mol−1·K−1[7] | ||
| Opasnost | |||
| Podaci o bezbednosti prilikom rukovanja (MSDS) | ICSC 0183 PCTL Safety Website | ||
| EU-klasifikacija | |||
| EU-indeks | 007-004-00-1 | ||
| NFPA 704 | |||
| R-oznake | R8 R35 | ||
| S-oznake | (S1/2) S23 S26 S36 S45 | ||
| Tačka paljenja | Nezapaljiva | ||
| Srodna jedinjenja | |||
| Drugi anjoni | Azotasta kiselina | ||
| Drugi katjoni | Natrijum nitrat Kalijum nitrat Amonijum nitrat | ||
| Srodna jedinjenja | Azot-pentoksid | ||
|
Ukoliko nije drugačije napomenuto, podaci se odnose na standardno stanje (25 °C, 100 kPa) materijala | |||
| Infobox references | |||
Azotna kiselina je veoma jaka neorganska kiselina molekulske formule HNO3. To je bezbojna, izuzetno kaustična i otrovna supstanca. Lako isparava, a pri koncentracijama većim od 86% često se naziva pušljiva azotna kiselina. U koncentrovanom obliku izuzetno je jako oksidaciono sredstvo. Prvi ju je sintetisao alhemičar Jabir ibn Hajan oko 9. veka nove ere. Soli ove kiseline nazivaju se nitrati.
Azotna kiselina u vodenom rastvoru u potpunosti disosuje do NO3- anjona i slobodnog protona koji se vezuje sa molekulima vode iz rastvora gradeći hidronijum jon (H3O+).[8][9][10]
Jako je oksidaciono sredstvo. Može da izreaguje čak i sa površinskim slojem plementih metala, zbog čega se koristi u spremanju carske vode, koja može da rastvara zlato i platinu. Na sobnoj temparaturi to je bezbojna tečnost koja lako isparava, pogotovu pri većim koncentracijama, odavajući žuta do crvenih isparenja.
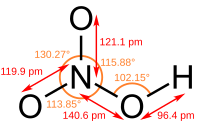
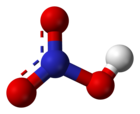
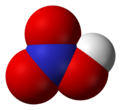
Azotna kiselina gradi veliki broj soli - nitrata - koji su veoma velika i važna grupa jedinjenja. Većina je polarna, te vrlo dobro rastvorna u polarnim rastvaračima, prvenstveno vodi i etanolu. Veze između azota i kiseonika (kako u kiselini tako i u nitratnoj grupi) su sve jednake dužine, sa sp2 hibridizovanim atomom azota, i uglom između veza od 120°, što odgovara planearnom obliku nitratne (nitro) grupe.
Azotna kiselina se može dobiti mešanjem azot (IV)-oksida sa vodom pri čemu se dobija smeša azotne i azotaste kiseline. Prečišćavanje ove smeše se najčešće vrši destilacijom sa sumpornom kiselinom, koja je higroskopna supstanca, pri čemu se povećava udeo azotne kiseline u rastvoru. Azotna kiselina industrijske jačine varira između 50-68%. U laboratoriji se može dobiti i dejstvom koncentrovane sumporne kiseline (H2SO4) na kalijum nitrat (KNO3), i naknadnom destilacijom na temperaturi ključanja nitratne kiseline (83 °C), pri čemu se izdvaja tzv. crvena pušljiva azotna kiselina (u gasnoj fazi) koju je moguće prevesti u konvencionalnu (belu) azotnu kiselinu. Pritom, u destilacionoj posudi ostaje kristalizovan kalijum hidrogensulfat (KHSO4)
Na industrijskom nivou, dobija se Ostvaldovim procesom, nazvanim po Vilhelmu Ostvaldu, oksidacijom amonijaka.
U laboratoriji, azotna kiselina je veoma važan reagens, dok je njena upotreba u industriji još značajnija. Koristi se u procesima dobijanja eksploziva (kao nitroglicerin, trinitrotoluen), veštačkih đubriva (amonijum nitrat), prečišćavanja metala u metalurgiji kao i u nekim organskim sintezama.
Bela pušljiva azotna kiselina (koja je praktično anhidrirana kiselina, teoretske ili približne jačine) koristi se kao oksidant u raketama na tečno gorivo.
U kontaktu sa kožom izaziva teške hemijske opekotine karakteristične žute boje, koja je proizvod reakcije kiseline sa jednim od proteina u koži - keratinom.
- ↑ Li Q, Cheng T, Wang Y, Bryant SH (2010). „PubChem as a public resource for drug discovery.”. Drug Discov Today 15 (23-24): 1052-7. DOI:10.1016/j.drudis.2010.10.003. PMID 20970519.
- ↑ Evan E. Bolton, Yanli Wang, Paul A. Thiessen, Stephen H. Bryant (2008). „Chapter 12 PubChem: Integrated Platform of Small Molecules and Biological Activities”. Annual Reports in Computational Chemistry 4: 217-241. DOI:10.1016/S1574-1400(08)00012-1.
- ↑ Hettne KM, Williams AJ, van Mulligen EM, Kleinjans J, Tkachenko V, Kors JA. (2010). „Automatic vs. manual curation of a multi-source chemical dictionary: the impact on text mining”. J Cheminform 2 (1): 3. DOI:10.1186/1758-2946-2-3. PMID 20331846.
- ↑ Joanne Wixon, Douglas Kell (2000). „Website Review: The Kyoto Encyclopedia of Genes and Genomes — KEGG”. Yeast 17 (1): 48–55. DOI:10.1002/(SICI)1097-0061(200004)17:1<48::AID-YEA2>3.0.CO;2-H.
- ↑ Gaulton A, Bellis LJ, Bento AP, Chambers J, Davies M, Hersey A, Light Y, McGlinchey S, Michalovich D, Al-Lazikani B, Overington JP. (2012). „ChEMBL: a large-scale bioactivity database for drug discovery”. Nucleic Acids Res 40 (Database issue): D1100-7. DOI:10.1093/nar/gkr777. PMID 21948594.
- ↑ Bell, R. P. (1973), The Proton in Chemistry (2nd izd.), Ithaca, NY: Cornell University Press
- ↑ 7,0 7,1 Zumdahl, Steven S. (2009). Chemical Principles 6th Ed.. Houghton Mifflin Company. str. A22. ISBN 978-0-618-94690-7.
- ↑ David L. Nelson, Michael M. Cox (2005). Principles of Biochemistry (4th izd.). New York: W. H. Freeman. ISBN 0-7167-4339-6.
- ↑ Lide David R., ur. (2006). CRC Handbook of Chemistry and Physics (87th izd.). Boca Raton, FL: CRC Press. 0-8493-0487-3.
- ↑ Susan Budavari, ur. (2001). The Merck Index: An Encyclopedia of Chemicals, Drugs, and Biologicals (13th izd.). Merck Publishing. ISBN 0-911910-13-1.
- Zumdahl, Steven S. (2009). Chemical Principles 6th Ed.. Houghton Mifflin Company. str. A22. ISBN 978-0-618-94690-7.
- NIOSH Pocket Guide to Chemical Hazards
- National Pollutant Inventory – Nitric Acid Fact Sheet
- Calculators: surface tensions Arhivirano 2020-02-22 na Wayback Machine-u, and densities, molarities and molalities Arhivirano 2020-02-22 na Wayback Machine-u of aqueous nitric acid


