Жива
Оваа статија можеби бара дополнително внимание за да ги исполни стандардите за квалитет на Википедија. Ве молиме подобрете ја оваа статија ако можете. |
 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Спектрални лининии на живата (УВ невидливи за човекот) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Општи својства | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Име и симбол | жива (Hg) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Изглед | сребреникав | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Живата во периодниот систем | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Атомски број | 80 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Стандардна атомска тежина (±) (Ar) | 200,592(3)[1] | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Категорија | преоден метал | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Група и блок | група 12, d-блок | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Периода | VI периода | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Електронска конфигурација | [Xe] 4f14 5d10 6s2 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
по обвивка | 2, 8, 18, 32, 18, 2 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Физички својства | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Фаза | течна | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Точка на топење | 234,3210 K (−38,8290 °C) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Точка на вриење | 629,88 K (356,73 °C) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Густина близу с.т. | 13,534 г/см3 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Тројна точка | 234,3156 K, 1,65×10−7 kPa | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Критична точка | 1.750 K, 172 MPa | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Топлина на топење | 2,29 kJ/mol | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Топлина на испарување | 59,11 kJ/mol | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Моларен топлински капацитет | 27,983 J/(mol·K) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
парен притисок
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Атомски својства | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Оксидациони степени | 4, 2 (живин), 1 (жива) (слаб базичен оксид) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Електронегативност | Полингова скала: 2 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Енергии на јонизација | I: 1.007,1 kJ/mol II: 1.810 kJ/mol II: 3.300 kJ/mol | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Атомски полупречник | емпириски: 151 пм | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Ковалентен полупречник | 132±5 пм | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Ван дер Валсов полупречник | 155 пм | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Разни податоци | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
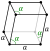
| Кристална структура | ромбоедрална | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Брзина на звукот | течност: 1.451,4 м/с (на 20 °C) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Топлинско ширење | 60,4 µм/(m·K) (при 25 °C) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Топлинска спроводливост | 8,30 W/(m·K) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Електрична отпорност | 961 nΩ·m (на 25 °C) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Магнетно подредување | дијамагнетно[2] | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| CAS-број | 7439-97-6 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Историја | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Откриен | Старите кинези и индијци (Пред 2.000 п.н.е) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Најстабилни изотопи | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Режимите на распад во загради се предвидени, но сè уште не се забележани | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Жива — хемиски елемент со симбол Hg и реден број 80. Таа претставува единствениот течен метал, а заедно со бромот се единствените природни елементи кои се наоѓаат во течна агрегатна состојба. Поради својството правилно да се шири со зголемување на температурата се користи во топломерите.
Живата има пронаоѓалишта низ целиот свет најмногу како цинабар (живен сулфид), кој е извор на црвениот пигмент вермилион и најмногу се добива од редукција на живениот сулфид. Цинабарот е многу токсичен со земање или инхалација на прашина. Позиционирањето на живата исто така може да резултира од изложеноста на формите на растворливот во вода (како живен хлорид или метилжива), инхалацијата на живена пареа или јадење на морска храна која е загадена со жива. Живата се користи во топломерите, барометрите, манометрите, сфигмоманометрите, пловните вентили, некои електрични прекинувачи и други научни апарати, но загриженоста за токсичноста на елементот водеа до исфрлање на топломерите и сфигмоманометрите од клиниките и воведување на алкохолните, дигиталните или термисторните инструменти. Таа останува во употреба во научните истражувања и во материјалите за заболекарско лечење. Таа се користи во осветлувањето: струјата поминува преку пареа од живата во фосфорна цевка и произведува краток бран ултравиолетова светлина која потоа предизвикува фосфорот на флуоросцентност, правејќи визуелна светлина.
Хемиски одлики
[уреди | уреди извор]Живата има исклучителна ниска температура на топење. Целосното објаснување на овој факт бара длабоко навлегување во квантната физика, но може да биде резимиран како: живата има единствена конфигурација на електроните каде што пополнувањето на нив е достапно во 1ѕ, 2ѕ, 2р, 3ѕ,3р, 4ѕ, 4р, 4d, 4f, 5s, 5p, 5d и 6s подќелии. Како таква конфигурацијата е многу отпорна на отстранувањето на електроните, живата се однесува слично како елементите кои се благородени гасови, чијашто форма ги ослабнува врските и на тој начин лесно се топат. Стабилноста на 6ѕ ќелијата се должи на присуството на пополнетата 4f ќелија. Отсуството на пополнетата f ќелија е причина за повисока температура на топење. Металите како златото имаат атоми со еден помалку 6ѕ електрон за разлика од живата. Тие елементи се полесни за отстранување и се поделени помеѓу атомите на златото формирајќи релативно силни метални врски. Со својата точка на топење (-38.86 степени), густината на живата е 13.534 g/cm3.
Реактивност и соедниненија
[уреди | уреди извор]Живата се раствора за да формира смеси со злато, цинк и многу други метали. Бидејќи железото е исклучок, железните шишиња се секогаш користени за пренесување на живата. Другите метали кои не формираат смеси со живата вклучувајќи го танталот, волфрам и платината. При загревање, живата исто така реагира со кислород за да формира жива оксид, кој потоа може да се разложува со понатамошно загревање на повисоки температури. Бидејќи живата се наоѓа под водородот во низата на реактивност на металите, живата не реагира со повеќето киселини, како што е сулфурната киселина, но оксидирањето на киселините како што е концентрираната сулфура киселина и азотната киселина се разложуваат на сулфатни, азотни и хлоридни соли. Како среброто, живата реагира со атмосферскиот водород. Живата дури и реагира со цврсти сулфурни лушпи, кои се користени за апсорбирање на пареата од живата. Некои важни соли на живата се: • Жива (I) хлорид понекогаш сè уште се користи во медицината, во оптичките филтри како стандарден во електрохемијата; • Живен експлозив, детонатор кој широко се користи во експлозивите; • Жива (II) оксид, главниот оксид на живата; • Жива (II) сулфид- пронаоѓан природно како рудата цинбар или вермилионот кој е вискоквалитетен обоен пигмент; • Жива (II) селенид, Жива (II) телурид, Жива кадмиум телурид и жива цинк телурид се полупроводници и материјали пронаоѓачи на инфраред. Во овие соединенија, живата покажува две состојби на оксидација: +1 и +2. Состојбата +1 содржи Hg2+; 2. Раствори на Hg2+2 се во рамнотежа со Hg2+ и металната жива:
Hg2+ + Hg Hg2+ 2 Оваа рамнотежа предизвикува раствори на Hg2+2 за да има мала количина на Hg2+ присутна. Земјаќи ја Hg2+ со друга реакција, како што е реагирање со јаки лиганди или учество во нерастворлива сол, ќе предизвика сите Hg2+ целосно да се диспропорционира во Hg2+ и елементна жива. Покрај Hg2+2, живата исто така формира други поликатјони на живата како што е Hg2+3. Повисоки состојби на оксидација на живата беа потврдени во септември 2007 година, со синтеза на жива (IV) флорид (HgF4) користејќи матрични техники на изолација. Лабораториските тестови покажаа дека електричното празнење предизвикува благородните гасови да се комбинираат со пареата на живата. Овие соединенија се споени заедно со van der Waals силите и резултираат во Hg•Ne, Hg•Ar, Hg•Kr, и Hg•Xe. Соединенијата на органската жива се исто така важни. Метил живата е опасно соединение кое е широко пронаоѓано како загадувач во водата, телата и реките. Живата брзо стапува во реакција со алуминиумот за да формира жива – алуминиум соединение, кога двата чисти метали дојдат до контакт. Меѓутоа, кога соединението е подложено на воздух, алуминиумот оксидира, напуштајќи ја живата. Оксидот се одделува, изложувајќи го повеќе соединението на живата кое го повторува процесот. Овој процес продолжува додека се потроши набавката на соединението. Бидејќи процесот ослободува жива, мала количина на жива може „изеде“ голема количина на алуминиум, со формирање на соединение и ослободувајќи го алуминиумот како оксид. Алуминиумот во воздух е заштитен со мал слој молекули од својот оксид, кој не е порозен на кислород. Живата кога дојде во контакт со оксид не е штетна, иако ако некој друг елемнтен алуминиум е изложен, живата може да се комбинира со него и може да го оштети алуминиумот. Поради оваа причина, ограничувањата се поставени на употребата и користењето на живата во близин�� на алуминиум. Живата не е дозволена во воздухопловството под повеќе околности поради ризикот од формирање соединение со некои алуминиумски делови во воздухопловството. Живата е пронајдена во Египетските гробишта кои датираат од 1500 година пред нашата ера. Таа исто така им беше позната и на древните кинези. Во Кина и Тибет, се мислело дека живата се користи за продолжување на животот, за лекување и генерално да го одржува доброто здравје. Еден кинески цар, Кин Ши Хуанг Ди – наводно изгорел во гробот во кој имало реки на течна жива, типично за реките во Кина – беше убиен со пиење жива и јака смеса од жад (предизвикувајќи инсуфуциенција на црниот дроб, труење и смрт на мозокот) за кои мислел дека ќе му дадат вечен живот. Старите Грци ја користеле живата во кремите (мастите); древните Египќани и Романци ја користеле во козметиката која понекогаш го деформирала лицето. До 500 година пред нашата ера живата била користена за правење смеси со други метали. Индијанскиот збор за алхемија е Rasavatam кој значи „патот на живата“. Алхемичарите ја мислеа живата како Главен Дел од која сите метали беа направени. Тие веруваа дека различните метали можат да бидат произведени со варирање на квалитетот и квантитетот на сулфурот кој се содржи во живата. Најчистиот метал од овие беше златото, и живата се бараше за обидите за преобразбата на основните метали во злато, што беше и цел на алхемичарите. Hg е нов хемиски симбол за живата. Тој доаѓа од hidrargyrum, латинизирана форма од грчкиот збор Жива (hidrargyrum), кој е сложен збор со значење „вода-сребро“ (hidr=вода, argyrum=сребро) – бидејќи таа е течна како водата и сјајна како среброто. Рудниците во Алмаден (Шпанија), Монте Амијата (Италија) и Идрија (сега Словенија) доминираа со производството на жива од отворањето на рудникот Алмаден, пред 2500 години сè додека не беа пронајдени нови наоѓалишта на крајот на 19 век. Живата е екстремно редок елемент во Земјината кора, имајќи просек од само 0.08 делови на милион. Меѓутоа бидејќи геохемиски не е измешана со оние елементи од кои се состои поголемиот дел масата на Земјината кора, живините руди можат одлично да бидат концентрирани земјаќи ја предвид застапеноста на елементот во обичен камен. Најбогатите живени руди содржат 2.5% жива по маса и дури и најслабо концентрираните наоѓалишта содржат најмалку 0.1% жива. Живените руди обично се јавуваат во многу млади рудни зони каде што карпите со голема густина се приближани до Земјината кора, често во жешки активации или други вулкански реакции. Започнувајќи во 1558 година, со пронаоѓањето на патио процесот за вадење на сребро од живена руда, живата стана суштествен ресурс во економијата на Шпанија и на нејзините Американски колонии. Живата беше употребувана за вадење на сребро од обилните рудници во Нова Шпанија и Перу. Најпрво, Шпанските рудници во Алмаден во Јужна Шпанија ја снабдуваа потребната жива за сите колонии. Наоѓалошта на жива беа пронајдени во Новиот Свет, и повеќе од 100.000 тони на жива беа извадени од регионот на Хуанкавелица, Перу, преку движење од три века следејќи го пронаоѓањето на наоѓалиштата таму во 1563 година. Патио процесот и подоцна и процесот на пан амалгамирање продолжија да ја задоволуваат големата побарувачка за жива за да се обработуваат сребрените руди сè до крајот на 19 век. Живата се вади со загревање на цинабар на нормален воздух и кондензирање на пареата. Равенката за оваа екстракција е: HgS + O2 → Hg + SO2 Во 2005 година, Кона беше најголемиот производител на жива со речиси две третини од глобалното производство а потоа е Казахстан. Неколку други земји имаат незапишано производство на жива од бакар со преработка на отпадни материи. Поради големата токсичност на живата, и вадењето на цинабарот од рудниците и рафинирањето на живата се опасни и историски случаи на труење со жива. Во Кина, затворениците биле користени од страна на приватна рудничка компанија, порано од 1950-тите, за да создадат нови ценабар живени рудници. Илјадници затвореници биле искористени од Луо Хи рудничката компанија за да ископаат тунели. Здравјето на работниците кои работат во рудниците е подложено на ризик. Директивата на Европската Унија која бара договор за правење на флуоросцентни светилки кои треба да бидат направени до 2012 година ја охрабри Кина повторно да ги отвори смртоносните цинабар рудници за да дојде до бараната жива за производство на CFL светилки. Како резултат на тоа, опасностите во животната средина беа проблем, особено во јужните делови на Фошан и Гуангзоу провинциите на југозапад. Напуштените рудници за жива често содржат и многу опасни отпадни печени цинабарни калцини. Отстранувањето на водата од ваквите места е познат извор за еколошка катастрофа. Претходните рудници на жива може да бидат соодветни за конструктивна повторна употреба. На пример, во 1976 година грофовијата Санта Клара, Калифорнија го купи историскиот Алмаден Квиксилвер рудникот и направи грофовски парк на таа локација, по спроведувањето на зголемена заштита и средински анализи на сопственоста. Природните извори, како што се вулканите, се главни виновници за емисиите на живата кои се речиси половина од атмосферата. Другата половина предизвикана од човекот може да биде поделена на следните пресметани проценти: • 65% од постојаното согорување, од што јаглените термоелектрани се најголемиот агрегатен извор (40% од Американските емисии на жива во 1999год). Ова ги вклучува и термоелектраните кои работат на гас каде што живата не се отстранува. Емисиите од јагленото согорување се меѓу еден и два реда поголеми од емисиите на согорувањето на масло, зависно од земјата. • 11% од производството на злато. Трите најголеми точки на извори за емисии на живата во Америка се трите најголеми рудници на злато. Хидрогеохемиското испуштање на жива од отпадите на рудниците за злато се сметаат како значаен извор на атмосферска жива во источна Канада. • 6,8% од производството на обоени метали, особено топилниците. • 6,4% од производството на цемент. • 3,0% од исфрлањето на отпадот, вклучувајќи комунален и опасен отпад, крематорија и палењето на отпадната кал. • 3,0% од производство на натриум хидроксид. • 1,4% од производството на сурово железо и челик. • 1,1% од производството на жива, особено за батерии. • 2,0% од други извори. Овие проценти се проценки од глобалните емисии на жива предизвикани од човекот во 2000 година, исклучувајќи го горењето на биомасата, еден многу важен проблем во некои региони. Моменталното атмосферско согорување на живата во надворешниот урбан воздух е (0.01-0.02 µg/m3 ) внатрешната концентрација е значајно крената над надворешната концентрација, во граница од 0.0065 – 0.523 µg/m3 (просек 0.069 µg/m3 ). Живата исто така навлегува во средината преку неправилно отстранување на одредени производи. Производи кои содржат жива се: авто делови, батерии, флуоросцентни светилки, медицински производи, топломери и термостати. Живините топломери сè уште понекогаш се користат на полето на медицината бидејќи тие се по исправни од алкохолните топломери, сепак и двата вида се заменети со електронски топломери. Живините топломери се сè уште широко користени за одредени научни шримени поради нивната поголема точност и граница на работа. Американскиот Акт за Чист Воздух, основана во 1990 година, ја стави живата на списокот на токсични загадувачи кои треба да бидат контролирани колку е можно повеќе. Така, индустриите кои ослободуваат големи концентрати на жива во средината се согласија да инсталираат технологии за постигнување на максимална контрола. Во 2005 година ЕРА правилникот ги додаде термоелектраните на списокот на извори кои треба да бидат контролирани. На државите и беше дадено до Ноември 2006 година да воспостават постриктна контрола и неколку држави го прават тоа. Правилото за Воздух Чист од Жива беше побиено од страна на Федералниот Апелационен Суд на 8 февруари 2008 година. Се мислеше дека правилото не е доволно добро за да го заштити здравјето на луѓето кои живеат во близина на термоелектраните на јаглен. Историски, едно од најголемите испуштања беше од Колекс погонот, сепарација на изотопи од литиум-погони во Оак Риџ. Записите не се целосни и јасни, но владините комисии проценија дека околу два милиони фунти на жива не се пресметани. Една од најлошите индустриски катастрофи во историјата беше предизвикана со испуштање на соединенија на живата во Минамата Заливот, Јапонија. Корпорацијата Чисо, компанија за ѓубре а подоцна и петрохемиска компанија, беше обвинета како одговорна за загадување на заливот од 1932 – 1968 година. Пресметано е дека преку 3.000 луѓе страдале од многу деформитети, неколку симптоми на труење од жива или смрт станаа познати како Минамата болест. Живата примарно се користи за изработка на индустриски хемикалии или за електрични и електронски примени. Се користи во некои топломери, особено во оние кои се користат за мерење на високи температури. Уште поголема количина се користи гасната жива во флуоросцентните светилки, додека најмногу во другите примени е намалена употребата на живата поради здравствени и безбедносни прописи и во некои примени е заменета со помалку токсични но многу пообемни Галенстан легури.
Медицина
[уреди | уреди извор]Живата и нејзините соединенија се користат и во медицината, иако денес тие помалку се користат за разлика од порано бидејќи токсичните ефекти на живата и нејзините соединенија се секаде познати. Елементарната жива е состојка на денталните соединенија. Тиомерсалот е органско соединение кое се користело како конзерванс во вакцините, но оваа употреба е исфрлена. Друго соединение на живата е Мерброминот, кој е тропски антисептик користен за мали посечоци и гребнатинки и денес сè уште се користи во некои земји. Жива (I) хлорид традиционално била користена како дијуретик, тропски дезинфектант и лаксатив. Живата (II) хлорид била користена и за лекување на сифилис (зедно со некои други соединенија на живата), иако тоа е толку токсично што некогаш симптомите на токсичноста биле помешувани со оние на сифилисот кои требало да се лечат. Исто така се користи и како дезинфектант. Сината маса, пилула или сируп во кој живата е главна состојка, била препишувана во 19 век за бројни состојби како: запек, депресија, при раѓање деца и за забоболки. Во раниот 20 век, живата им била давана на децата годишно како лаксатив и средство за чистење од вошки и била користена во пудрите кои се користеле при никнувањето на забите кај децата. Живата која содржи органохалиден мербромин (некогаш продаван како Живохром) сè уште широко се користи но во некои земји е забранета, како на пример, во Америка. Во 1930-тите некои вакцини содржеле тиомерсал, кој е метаболизиран или разложен на етил жива. Иако многу се шпекулирало дека овој конзерванс заснован на жива може да предизвика аутизам кај децата, ниту едно испитување не покажа дека ова е вистина. Меѓутоа, тиомерсалот беше отстранет или намален на многу мали количини во вакцините во Америка кои се препорачани за деца кои се на 6 годишна возраст и помали, со исклучок на неактивната вакцина против грип. Живата во формата на нејзините руди, цинабар, останува сè уште важна компонента во кинеската, тибетската и ајурведската медицина. Бидејќи можат да настанат проблеми кога овие лекови се извезувани во земји каде што е забранета употребата на жива во лековите, во денешни времиња, додадени се по нетоксични замени за живата. Денес употребата на живата во медицината е забранета, особено во развиените земји. Топломерите и сфигмоманометрите кои содржат жива биле измислени во почетокот на 18 век и крајот на 19 век. На почетокот на 21век нивната употреба е одбиена а во некои земји и забранета, во државните и медицинските институции. Во 2002 година Сенатот на Америка постави регулатива за исфрлање на продажбата на живини топломери. Во 2003 година, Вашингтон и Мајна станаа првите држави кои ги забранија апаратите за мерење притисок кои содржеа жива. Соединенија на живата се пронајдени во некои лекови кои се продаваат без рецепти, вклучувајќи тропски антицептици, стимулативни лаксативи, капки за очи и спрејови за нос. Прехранбената и Лекарска Администрација ги „онеспособија податоците за да утврдат генерално признание на безбедноста и делотворноста“ на живините состојки во овие производи. Живата сè уште се користи во некои диуретици, иако постојат и други субститути кои се покорисни.
Козметика
[уреди | уреди извор]Живата, како тиомерсал, многу се користи во производството ма маскари. Во 2008 година, Минесота беше првата држава која во Америка која го забрани додавањето на живата во козметиката, давајќи понепристапен стандард дури и од федералната влада. Биомониторингот заснован на популацијата исто така покажа дека нивоата на концентрираност на живата се повисоки кај консумирачите на морска храна и на храна од риба.
Производство на хлор и сода бикарбона
[уреди | уреди извор]Хлорот е произведен од натриум хлорид кој користи електролити за да го одвои металниот натриум од гасот на хлорот. Обично солта е растворена во вода за да се добие саламура. Куповните производи кои се произведени од секакви хлоралкални процеси се водород (Н2) и натриум хидроксид (NaOH), којшто е наречен сода бикарбона или алкален раствор. До сега најголемата употреба на живата на крајот на 20 век беа живените процеси во клетките (исто така наречени Кастнер – Келер процеси) каде што металниот натриум е формиран како соединение на катода направена од жива; овој натриум потоа е ставан во реакција со вода за да произведе натриум хидроксид. Многу од индустриските исфрлања на живата во 20 век настанаа од овој процес, иако современите постројки тврдеа дека во овој поглед живата е безбедна. После 1985 година, сите нови хлоралкални производни институции кои беа изградени во Америка користеа технологии на клеточни мембрани или клеточни дијафрагми за да произведат хлор.
Вадење на златото и среброто од рудниците
[уреди | уреди извор]Во историјата, живата беше многу користена во хидрауличното вадење на златото од рудниците со цел да се помогне за златото да пропаѓа низ следната мешавина на вода и чакал. Малите парчиња жива можат да формираат соединение на жива и злато и со тоа да ги зголемат границите на обновување на златото. Големата скала на употреба на живата престана во 1960-тите. Меѓутоа, живата сè уште се користи во мали количини. Проценето е дека 45.000 метрички тони на жива, користени во Калифорнија за плацерно вадење на руда, не биле обновени. Живата исто така е користена и во вадење на сребро од рудниците.
Останата употреба
[уреди | уреди извор]Гасната жива се користи во светилките кои работат на живена пареа, во некои неонки и во флуоросцентните светилки. Овие нископритисочни светилки емитираат многу спектрални тенки линии, кои традиционално се користат во оптичната спектроскопија. Трговските калибрациски светилки се продавани за оваа цел; меѓутоа едноставното рефлектирање на некои од флуоросцентните плафонски светилки во спектрометрот се заедничка калибрациска употреба. Гасовитата жива, исто така, ја има во некои електронски цевки, како игнитрони, тиратрони. Исто така, таа е користена во специјалистичките светилки во медицинска нега за тенот на кожата и за дезинфекција. Гасната жива е додадена и во светилките кои се наполнети со златни аргонски катоди за да ја зголемат јонизацијата и електричната спроводливост. Светилка наполнета со аргон без жива ќе има мрачни дамки и ќе ја испушта светлината правилно. Кога живата се додава во цевките на неонките, произведената светлина има непостојани црвени/сини дамки, додека главниот процес на запалување не биде завршен; на крајот таа се пали со постојана слаба сина боја. Некои медицински топломери, особено оние за високи температури, се наполнети со жива; меѓутоа, тие постепето исчезнуваат. Во САД, непрепишуваните топломери за температура се забранети уште од 2003 година. Течната жива е дел од популарната електрода со секундарна употреба (наречена каломел електрода) во електрохемијата како алтернатива на стандардната водородна електрода. Каломелската електрода се користи за изработка на електродниот потенцијал. Последно, но не најнезначајно, тројната точка на живата, -38.8344 степени, е фиксирана точка користена како температурен стандард на Меѓународната Скала на Температурата (ITS-90).
Живата како тема во уметноста и во популарната култура
[уреди | уреди извор]- „Труење со жива“ (Mercury Poisoning) - песна на англискиот рок-пејач Греам Паркер (Graham Parker) од 1979 година.[3]
Наводи
[уреди | уреди извор]- ↑ Standard Atomic Weights 2013. Commission on Isotopic Abundances and Atomic Weights
- ↑ „Mgnetic Susceptibility of the Elements And Inorganic Compounds“ (PDF). http://www-d0.fnal.gov/. Fermi National Accelerator Laboratory: DØ Experiment (lagacy document). Архивирано од изворникот (PDF) на 2004-03-24. Посетено на 18 February 2015. Надворешна врска во
|website=(help) - ↑ YouTube, Graham Parker & The Rumour - Squeezing Out Sparks (1979) (пристапено на 19.12.2017)
| Периоден систем на елементите | |||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 | 11 | 12 | 13 | 14 | 15 | 16 | 17 | 18 | ||||||||||||||||
| I | H | He | |||||||||||||||||||||||||||||||
| II | Li | Be | B | C | N | O | F | Ne | |||||||||||||||||||||||||
| III | Na | Mg | Al | Si | P | S | Cl | Ar | |||||||||||||||||||||||||
| IV | K | Ca | Sc | Ti | V | Cr | Mn | Fe | Co | Ni | Cu | Zn | Ga | Ge | As | Se | Br | Kr | |||||||||||||||
| V | Rb | Sr | Y | Zr | Nb | Mo | Tc | Ru | Rh | Pd | Ag | Cd | In | Sn | Sb | Te | I | Xe | |||||||||||||||
| VI | Cs | Ba | La | Ce | Pr | Nd | Pm | Sm | Eu | Gd | Tb | Dy | Ho | Er | Tm | Yb | Lu | Hf | Ta | W | Re | Os | Ir | Pt | Au | Hg | Tl | Pb | Bi | Po | At | Rn | |
| VII | Fr | Ra | Ac | Th | Pa | U | Np | Pu | Am | Cm | Bk | Cf | Es | Fm | Md | No | Lr | Rf | Db | Sg | Bh | Hs | Mt | Ds | Rg | Cn | Nh | Fl | Mc | Lv | Ts | Og | |
|
| |||||||||||||||||||||||||||||||||
| ||||||||||||||||
|