இசுட்ரோன்சியம் ஆக்சைடு

| |
| |
| பெயர்கள் | |
|---|---|
| ஐயூபிஏசி பெயர்
இசுட்ரோன்சியம் ஆக்சைடு
| |
| வேறு பெயர்கள்
இசுட்ரோன்சியா
| |
| இனங்காட்டிகள் | |
| 1314-11-0 | |
| EC number | 215-219-9 |
InChI
| |
| யேமல் -3D படிமங்கள் | Image |
| பப்கெம் | 73975 |
| |
| பண்புகள் | |
| SrO | |
| வாய்ப்பாட்டு எடை | 103.619 கிராம்/மோல் |
| தோற்றம் | நிறமற்றது, கனசதுர படிகங்கள் |
| அடர்த்தி | 4.70 கிராம்/செ.மீ3 |
| உருகுநிலை | 2,531 °C (4,588 °F; 2,804 K) |
| கொதிநிலை | 3,200 °C (5,790 °F; 3,470 K) (சிதையும்) |
| வினைபடும் Sr(OH)2 | |
| கரைதிறன் | பொட்டாசியம் ஐதராக்சைடில் கலக்கும் ஆல்ககாலில் சிறிது கரையும் அசிட்டோன் மற்றும் ஈதரில் கரையாது. |
| −35.0•10−6 செ.மீ3/மோல் | |
| ஒளிவிலகல் சுட்டெண் (nD) | 1.810 [2] |
| கட்டமைப்பு | |
| படிக அமைப்பு | ஆலைட்டு (கனசதுரம்), cF8 |
| புறவெளித் தொகுதி | Fm3m, No. 225 |
| ஒருங்கிணைவு வடிவியல் |
எண்முகம் (Sr2+); எண்முகம் (O2−) |
| வெப்பவேதியியல் | |
| Std enthalpy of formation ΔfH |
-592.0 கிலோ யூல்•மோல்−1 |
| நியம மோலார் எந்திரோப்பி S |
57.2 யூல்•மோல் −1•கெல்வின்−1 |
| வெப்பக் கொண்மை, C | 44.3 யூல்•மோல்−1•கெல்வின்−1 |
| தீங்குகள் | |
| தீப்பற்றும் வெப்பநிலை | தீப்பற்றாது |
| தொடர்புடைய சேர்மங்கள் | |
| ஏனைய எதிர் மின்னயனிகள் | இசுட்ரோன்சியம் சல்பைடு |
| ஏனைய நேர் மின்அயனிகள் | பெரிலியம் ஆக்சைடு மக்னீசியம் ஆக்சைடு கால்சியம் ஆக்சைடு பேரியம் ஆக்சைடு |
மாறுதலாக ஏதும் சொல்லவில்லை என்றால் கொடுக்கப்பட்ட தரவுகள் யாவும் பொருள்கள் அவைகளின் இயல்பான வெப்ப அழுத்த நிலையில் (25°C, 100kPa) இருக்கும். | |
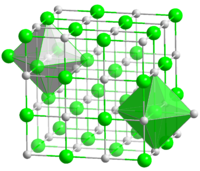
இசுட்ரோன்சியம் ஆக்சைடு (Strontium oxide) என்பது SrO என்ற மூலக்கூற்று வாய்ப்பாடு கொண்ட ஒரு கனிம வேதியியல் சேர்மமாகும். இசுட்ரோன்சியா என்ற பெயராலும் இச்சேர்மத்தை அழைப்பர். இசுட்ரோன்சியம் ஆக்சிசனுடன் வினைபுரிவதால் இசுட்ரோன்சியம் ஆக்சைடு உருவாகிறது. இசுட்ரோன்சியம் காற்றில் எரியும்போது இசுட்ரோன்சியம் ஆக்சைடும், இசுட்ரோன்சியம் நைட்ரைடும் சேர்ந்த கலவை தோன்றுகிறது. இசுட்ரோன்சியம் கார்பனேட்டு சிதைவடைவதாலும் இசுட்ரோன்சியம் ஆக்சைடு உருவாகிறது. இச்சேர்மம் ஒரு கார ஆக்சைடு வகையைச் சேர்ந்ததாகும்.
பயன்கள்
[தொகு]கிட்டத்தட்ட எதிர்மின் கதிர்க்குழாயின் எடையில் 8% இசுட்ரோன்சியம் ஆக்சைடு பயன்படுகிறது. 1970 ஆம் ஆண்டுகளிலிருந்து இசுட்ரோன்சியத்தின் முக்கியமான பயனாக இதுவே இருந்துவருகிறது[3]. வண்ண எதிர்மின் கதிர்க்குழாய் பயன்படுத்தப்படும் வண்ணத் தொலைக்காட்சிகள் மற்றும் இதர பொருட்களை விற்பதற்கு அமெரிக்காவில் சட்டப்பூர்வமான அங்கீகாரம் தேவையாகும். இக்கருவிகளிலிருந்து வெளிப்படும் எக்சு கதிர்களை தடை செய்ய இசுட்ரோன்சியத்தை பயன்படுத்த இந்த அங்கீகாரம் கோரப்பட்டது. குழாயின் கழுத்து, புனல் பகுதிகளில் ஈய(II) ஆக்சைடை பயன்படுத்த முடியும். ஆனால் இதை முகப்புத் தகடுகளில் பயன்படுத்துகையில் நிறச்சிதைவுக்கு காரணமாகிறது[4]
வினைகள்
[தொகு]வெற்றிடத்தில் இசுட்ரோன்சியம் ஆக்சைடுடன் அலுமினியத்தைச் சேர்த்து சூடாக்கினால் தனிமநிலை இசுட்ரோன்சியம் உருவாகிறது[1].
மேற்கோள்கள்
[தொகு]- ↑ 1.0 1.1 Lide, David R. (1998). Handbook of Chemistry and Physics (87 ed.). Boca Raton, FL: CRC Press. pp. 4–87. ISBN 0-8493-0594-2.
- ↑ Pradyot Patnaik. Handbook of Inorganic Chemicals. McGraw-Hill, 2002, பன்னாட்டுத் தரப்புத்தக எண் 0-07-049439-8
- ↑ Ober, Joyce A.; Polyak, Désirée E. "Mineral Yearbook 2007:Strontium" (PDF). United States Geological Survey. Retrieved 2009-09-14.
- ↑ Méar, F; Yot, P; Cambon, M; Ribes, M (2006). "The characterization of waste cathode-ray tube glass.". Waste management 26 (12): 1468–76. doi:10.1016/j.wasman.2005.11.017. பன்னாட்டுத் தர தொடர் எண்:0956-053X. பப்மெட்:16427267.
