1-Нафтол
| 1-Нафтол | |||
|---|---|---|---|
| |||
| Общие | |||
| Хим. формула | C10H8O | ||
| Физические свойства | |||
| Молярная масса | 144,16 г/моль | ||
| Плотность | 1,224 г/см³ | ||
| Энергия ионизации | 7,76 эВ[1] | ||
| Термические свойства | |||
| Температура | |||
| • плавления | 96,1 °C | ||
| • кипения | 288 (возг.) °C | ||
| • вспышки | 148 °C | ||
| Классификация | |||
| Рег. номер CAS | 90-15-3 | ||
| PubChem | 7005 | ||
| Рег. номер EINECS | 201-969-4 | ||
| SMILES | |||
| InChI | |||
| ChEBI | 10319 | ||
| ChemSpider | 6739 | ||
| Приведены данные для стандартных условий (25 °C, 100 кПа), если не указано иное. | |||
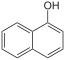
1-Нафто́л (α-нафтол, 1-оксинафталин) — органическое соединение с химической формулой C10H8O, представитель класса нафтолов, вместе с 2-нафтолом является одним из двух возможных изомеров мононафтола. Используется как промежуточный продукт в органическом синтезе.
Физические свойства
[править | править код]Белые или желтоватые кристаллы со слабым запахом фенола. Молярная масса — 144,16 г/моль. Температура плавления = 96,1 °C, кипения = 288 °C (с возгоранием), вспышки = 148 °C. Относительная плотность = 1,224. Растворим в спирте, хлороформе, ацетоне, растворах щелочей. Плохо растворим в воде[2][3].
Химические свойства
[править | править код]Проявляет свойства фенолов. Образует водорастворимые соли в растворах щелочей, ацетильные производные с ангидридами и хлорангидридами, эфиры со спиртами в присутствии сильных кислот (например, соляной или серной)[3].
Вступает в реакцию Бухерера-Лепти: при нагревании с бисульфитом натрия и аммиаком образуется бисульфитное производное, которое, реагируя с избытком аммиака, превращается в 1-нафтиламин[3].
Легко вступает в реакции электрофильного замещения[3].
При галогенировании[3]:
- гипохлоритом натрия образует 2-хлор-1-нафтол;
- сульфурилхлоридом образует 4-хлор-1-нафтол.
При сульфировании[3]:
- концентрированной серной кислотой даёт 1-гидроксинафталин-2-сульфокислоту с примесями 4-гидроксинафталин-1-сульфокислоты;
- двойным эквивалентом концентрированной серной кислотой даёт 4-гидроксинафталин-1,3-дисульфокислоту.
При нитровании концентрированной азотной кислотой[3]:
- в среде уксусной кислоты нитрогруппа входит в положение 2;
- в среде хлороформа нитрогруппа входит в положение 2 и 4.
1-Нафтол сочетается с диазосоединениями сначала по положению 4, затем — по положению 2[3].
При гидрировании 1-нафтола[3]:
- в кислой среде при температуре 70 °C и давлении 0,3 МПа с использованием платинового катализатора даёт 5-гидрокситетралин;
- в щелочной среде с использованием никелевого или палладиево-угольного катализатора при температуре 60—70 °C и давлении 1,2—1,4 МПа даёт 1-гидрокситетралин.
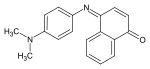
В процессе цветного фотографического проявления может использоваться как цветообразующая компонента, образуя индофеноловые красители. В частности, в случае использования в качестве цветного проявляющего вещества N,N-диметил-п-фенилендиамина образуется индофеноловый синий[4]:
Несмотря на то, что 1-нафтол не является проявляющим веществом классической структуры, про него известно, что он может проявлять хлоросеребряные фотобумаги, а в сильнощелочных растворах он окисляется до активных проявляющих веществ, таких как нафтогидрохинон и димерный 4,4’-дигидроксибинафтил[5].
Нахождение в природе
[править | править код]В небольших количествах содержится в каменноугольной смоле[6].
Получение
[править | править код]Получают[2]:
- гидролизом 1-нафтиламина;
- окислением тетралина, затем получившийся тетралон дегидрируют.
Применение
[править | править код]Используется в органическом синтезе для получения нафтолсульфокислот, галогенных и нитро- производных нафтолов. Также используется в производстве азокрасителей[2].
Применялся в фотографии как голубая диффундирующая цветообразующая компонента[7].
От 1-Нафтола получают реактив в микроскопии 2,4-Дихлор-1-нафтол.
Примечания
[править | править код]- ↑ David R. Lide, Jr. Basic laboratory and industrial chemicals (англ.): A CRC quick reference handbook — CRC Press, 1993. — ISBN 978-0-8493-4498-5
- ↑ 1 2 3 Кнунянц, 1983.
- ↑ 1 2 3 4 5 6 7 8 9 Карпова, 1992.
- ↑ Eaton, 1965, с. 54.
- ↑ Джеймс, 1980, с. 328.
- ↑ Огибин, 2013.
- ↑ Чельцов, 1958, с. 23, 49.
Литература
[править | править код]- Джеймс Т. Теория фотографического процесса = The theory of the photographic process / пер. 4-го американского изд. под ред. Картужанского А. Л.. — 2-е русское изд. — Л.: «Химия». Ленинградское отделение., 1980. — 672 с.
- Карпова Н. Б. Нафтолы : статья // Химическая энциклопедия / Гл. ред. Кнунянц И. Л. — М. : Большая Российская энциклопедия, 1992. — Т. 3. — С. 198. — 639 с.
- 1-Нафтол : статья // Химический энциклопедический словарь / Гл. ред. Кнунянц И. Л. — М. : Советская энциклопедия, 1983. — С. 368. — 792 с.
- Чельцов В.С., Бонгард С.А. Цветное проявление трехслойных светочувствительных материалов. — М.: Искусство, 1958.
- Eaton G. Photographic chemistry in black-and-white and color photograpy (неопр.). — second edition. — N. Y.: Morgan & Morgan, Inc., Publishers Hastings-on-Hudson, 1965.
Ссылки
[править | править код]- Нафтолы : [арх. 4 сентября 2022] / Ю. Н. Огибин // Нанонаука — Николай Кавасила. — М. : Большая российская энциклопедия, 2013. — С. 163. — (Большая российская энциклопедия : [в 35 т.] / гл. ред. Ю. С. Осипов ; 2004—2017, т. 22). — ISBN 978-5-85270-358-3.