Վիքիպեդիայից՝ ազատ հանրագիտարանից
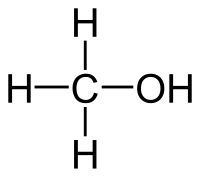
| Մեթիլալկոհոլ |
|---|
 |
 |
 |
| Ընդհանուր տեղեկություններ |
|---|
| Դասական անվանակարգում | մեթիլալկոհոլ |
|---|
| Ավանդական անվանում | Մեթիլսպիրտ, մեթանոլ |
|---|
| Քիմիական բանաձև | CH₄O |
|---|
| Ֆիզիկական հատկություններ |
|---|
| Ագրեգատային վիճակ | հեղուկ |
|---|
| Մոլային զանգված | 5,3E−26 կիլոգրամ[1] գ/մոլ |
|---|
| Խտություն | 0,79 ± 0,01 գ/սմ³[2] գ/սմ³ |
|---|
| Դինամիկ մածուցիկություն | 0,000544 ± 1,0E−6 պուազեյլ Պա/վ |
|---|
| Իոնիզացման էներգիա | 10,84 ± 0,01 Էլեկտրոն-վոլտ[2] և 1,7E−18 ջոուլ[3] կՋ/մոլ |
|---|
| Ջերմային հատկություններ |
|---|
| Հալման ջերմաստիճան | −144 ± 1 ℉[2], −98 °C[4] և −97,68 °C[3] °C |
|---|
| Եռման ջերմաստիճան | 147 ± 1 ℉[2], 65 °C[5] և 64,6 °C[3] °C |
|---|
| Այրման ջերմաստիճան | 52 ± 1 ℉[2] |
|---|
| Բռնկման ջերմաստիճան | +363 °C °C |
|---|
| Ինքնաբռնկման ջերմաստիճան | 440 °C |
|---|
| Եռյակ կետ | 175,45 K (−97,7°C) |
|---|
| Կրիտիկական ճնշում | 513,15 K (240 °C), 7,85 բար մթն. |
|---|
| Մոլյար ջերմատարողություն | 1,197 Ջ/(մոլ•Կ) |
|---|
| Գոյացան էնթալպիա | −234,8 կՋ/մոլ |
|---|
| Հալման էնթալպիա | 3167,29 ± 0,01 ջոուլ մեկ մոլի համար կՋ/մոլ |
|---|
| Եռման էնթալպիա | 37 400 ջոուլ մեկ մոլի համար կՋ/մոլ |
|---|
| Գոլորշու ճնշում | 13 020 ± 1 Pa և 96 ± 1 mm Hg[2] |
|---|
| Քիմիական հատկություններ |
|---|
| pKa | 15,5 ± 0,1[6][7] |
|---|
| Դիպոլ մոմենտ | 5,5E−30 Կլ·մ և 5,7E−30 Կլ·մ[3] |
|---|
| Դասակարգում |
|---|
| CAS համար | 67-56-1 |
|---|
| PubChem | 887 |
|---|
| EINECS համար | 200-659-6 |
|---|
| SMILES | CO |
|---|
| ЕС | 200-659-6 |
|---|
| RTECS | PC1400000 |
|---|
| ChEBI | 864 |
|---|
| Թունավորություն |
|---|
| Թունավորություն |    |
|---|
| IDLH | 7860 ± 10 mg/m³[2][6] |
|---|
| Եթե հատուկ նշված չէ, ապա բոլոր արժեքները բերված են ստանդարտ պայմանների համար (25 °C, 100 կՊա) |
Մեթիլալկոհոլ, մեթիլսպիրտ, մեթանոլ, փայտի սպիրտ, CH₃OH, հագեցած միատոմ սպիրտների պարզագույն ներկայացուցիչը։
Թույլ սպիրտային հոտով, անգույն հեղուկ է, հալման ջերմաստիճանը՝ -97,88°С, եռմանը՝ 64,5°С, խտությունը՝ 792,4 կգ/մ (20°С)։ Մեթիլալկոհոլի գոլորշիները օդի հետ առաջացնում են պայթուցիկ խառնուրդներ (6,72-35,5 ծավալ %), որոնց բոցավառման ջերմաստիճանն է 15,6°С։ Անսահման քանակներով լուծվում է ջրում և բազմաթիվ օրգանական լուծիչներում։ Ունի միատոմ սպիրտների բոլոր հատկությունները։
Արդյունաբերության մեջ ստացվում է ածխածնի (II) օքսիդից և ջրածնից։ Մրջնալդեհիդի, էսթերների (օրինակ, դիմեթիլ-տերեֆտա-լատ), ալկիլհալոգենիդների և այլ նյութերի արտադրության հումք է։ Մեթիլալկոհոլը ուժեղ թույն է, ազդում է նյարդային և անոթային համակարգերի վրա։ 5-10 մլ խմելու դեպքում առաջանում է ծանր թունավորում, կուրություն, իսկ 30 մլ-ի դեպքում՝ մահ։
Այս սպիրտն անվանվում է նաև փայտի սպիրտ, քանի որ փայտի չոր թորման արգասիք է։ Ստացվում է բարձր ջերմաստիճանում՝ ցինկքրոմային կատալիզատորի առկայությամբ CO–ի և ջրածնի փոխազդեցությունից.


- ↑ 1,0 1,1 methanol
- ↑ 2,00 2,01 2,02 2,03 2,04 2,05 2,06 2,07 2,08 2,09 2,10 http://www.cdc.gov/niosh/npg/npgd0397.html
- ↑ 3,0 3,1 3,2 3,3 3,4 3,5 3,6 David R. Lide, Jr. Basic laboratory and industrial chemicals: A CRC quick reference handbook — CRC Press, 1993. — ISBN 978-0-8493-4498-5
- ↑ 4,0 4,1 Bradley J., Williams A. J., Andrew S.I.D. Lang Jean-Claude Bradley Open Melting Point Dataset // Figshare — 2014. — doi:10.6084/M9.FIGSHARE.1031637.V2
- ↑ 5,0 5,1 GESTIS database
- ↑ 6,0 6,1 Ballinger P., Long F. A. Acid Ionization Constants of Alcohols. II. Acidities of Some Substituted Methanols and Related Compounds 1,2 // J. Am. Chem. Soc. / P. J. Stang — ACS, 1960. — Vol. 82, Iss. 4. — P. 795—798. — ISSN 0002-7863; 1520-5126; 1943-2984 — doi:10.1021/JA01489A008
- ↑ https://www.lachimie.org/docs/org/ch8_alcools_phenols_thiols.pdf — P. 11.
|
|---|
| | Ալիֆատիկ միատոմ սպիրտներ | |
|---|
| | Չհագեցած ալիլային թթուներ | |
|---|
| | Ալիցիկլիկ հագեցած միատոմ սպիրտներ | |
|---|
| | Ալիցիկլիկ չհագեցած միատոմ սպիրտներ | |
|---|
| | Արոմատիկ միատոմ սպիրտներ | |
|---|
| | Երկատոմ և եռատոմ սպիրտներ | |
|---|
| | Բազմատոմ սպիրտներ | |
|---|
|
| |
|---|
| | Բառարաններ և հանրագիտարաններ | |
|---|
| |
|
Այս հոդվածի կամ նրա բաժնի որոշակի հատվածի սկզբնական կամ ներկայիս տարբերակը վերցված է Քրիեյթիվ Քոմմոնս Նշում–Համանման տարածում 3.0 (Creative Commons BY-SA 3.0) ազատ թույլատրագրով թողարկված Հայկական սովետական հանրագիտարանից (հ․ 7, էջ 379)։ 
|








