Naatriumatsetaat

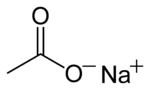 Naatriumetanaat ehk naatriumatsetaat on keemiline ühend valemiga C2H3NaO2. Tema lihtsustatud struktuurivalem on CH3COONa) ja ta on etaanhappe naatriumisool.
Naatriumetanaat ehk naatriumatsetaat on keemiline ühend valemiga C2H3NaO2. Tema lihtsustatud struktuurivalem on CH3COONa) ja ta on etaanhappe naatriumisool.
Naatriumetanaat on valge vees lahustuv lõhnatu pulber. Tema tihedus on 1528 kg/m³, sulamistemperatuur on 324 °C ja keemistemperatuur 881,4 °C. Tema molaarmass on 82,03 g/mol. Vees lahustub teda 0 °C juures 362 g/l, 20 °C juures 464 g/l, 60 °C juures 1390 g/l ja 100 °C juures 1701,5 g/l. Tema leekpunkt on 250 °C ja isesüttimistemperatuur 607 °C. Normaaltingimustes on ta stabiilne, peab vastu isegi tuleleegile, ja veega ta ka ei reageeri. Tema sattumine nahale põhjustab kerget ärritust, aga suuremat kahju ei sünni sellestki.
Naatriumetanaattrihüdraadi C2H3NaO2*3H2O tihedus on 1450 kg/m³, sulamistemperatuur on 58 °C, keemistemperatuur on 122 °C ja lahustuvus etanoolis 53 g/l.
Naatriumetanaati kasutatakse paljudel aladel, näiteks tekstiilitööstuses väävelhappe neutraliseerimiseks, toiduainetööstuses vürtsina ja biokeemias püsiva pH hoidmiseks. Seda kasutatakse ka soojenduspatjades, kus naatriumetanoaadi kristalliseerumisel eraldub soojus.
Keemilised omadused
[muuda | muuda lähteteksti]Naatriumetanaat on odav. Loomulikult saab seda valmistada laboris, kuid harilikult ostetakse seda keemiliste ainete tarnijatelt. Seda valmistatakse etaanhappe reaktsioonil naatriumkarbonaadi, naatriumvesinikkarbonaadi või naatriumhüdroksiidiga. Reaktsiooni käigus tekivad naatriumetanaat ja vesi ning kahel esimesel juhul ka süsihappegaas, mis eraldub muulidena, välja arvatud juhul, kui reaktsioon toimub hermeetilises anumas.
Äädika ja küpsetussooda vahel toimub järgmine keemiline reaktsioon:
CH3COOH + NaHCO3 -> CH3COONa + H2O + CO2.
84 g keedusoola reaktsioonil 750 ml 8% äädikaga tekib vette 82 g naatriumetanaati. Kui suurem osa veest ära keeta, võib saada kas naatriumetanaadi kontsentreeritud lahuse või naatriumetanaadi kristallid.
Naatriumetanaati saab kasutada estrite saamiseks alküülhaliididega. Näiteks reaktsioon bromoetaaniga:
CH3COONa + CH3CH2Br -> CH3COOCH2CH3 + NaBr.
Sellises reaktsioonis kasutatakse tavaliselt karboksüülrühma keemilise aktiivsuse suurendamiseks katalüsaatorina tseesiumi.
Väävelhappega reageerides moodustab naatriumetanaat naatriumsulfaadi ja etaanhappe:
2CH3COONa + H2SO4 -> 2CH3COOH + Na2SO4.
