HeLa




HeLa (/ˈhiːlɑː/; cũng được gọi là Hela hoặc hela) là một dòng tế bào bất tử được sử dụng trong nghiên cứu khoa học. Đây là dòng tế bào lâu đời nhất và được sử dụng phổ biến nhất ở người.[1][2] Dòng này có nguồn gốc từ các tế bào ung thư cổ tử cung được lấy ra vào ngày 8 tháng 2 năm 1951,[3] từ Henrietta Lacks, một bà mẹ 31 tuổi người Mỹ gốc Phi có 5 đứa con, qua đời vì bệnh ung thư vào ngày 4 tháng 10 năm 1951, và dòng tế bào này được đặt theo tên của Henrietta Lacks bằng cách lấy 2 ký tự đầu của tên riêng kết hợp với 2 ký tự đầu của họ mà tạo thành - HeLa.[4] Dòng tế bào này được phát hiện là có độ bền và khả năng sinh sản đáng kể, cho phép nó được sử dụng rộng rãi trong nghiên cứu khoa học.[5][6]
Các tế bào từ khối u ung thư cổ tử cung của Lacks đã được lấy đi mà cô không hề hay biết, đây là thông lệ ở Hoa Kỳ vào thời điểm đó.[7] Nhà sinh học tế bào George Otto Gey phát hiện ra rằng chúng có thể được giữ sống[8] và phát triển thành một dòng tế bào nếu được nuôi trong môi trường thích hợp. Trước đây, các tế bào được nuôi cấy từ các tế bào khác của con người sẽ chỉ tồn tại được vài ngày, nhưng các tế bào từ khối u của Lacks lại có thể sống và sinh sản không ngừng.
Lịch sử
[sửa | sửa mã nguồn]Nguồn gốc
[sửa | sửa mã nguồn]Năm 1951, một bệnh nhân tên Henrietta Lacks được đưa vào Bệnh viện Johns Hopkins với triệu chứng chảy máu âm đạo bất thường, và sau đó được điều trị ung thư cổ tử cung.[9] Lần điều trị đầu tiên của cô được thực hiện bởi Lawrence Wharton Jr., người lúc này đã thu thập các mẫu mô từ cổ tử cung của cô mà không có sự đồng ý của cô.[10] Sinh thiết cổ tử cung của cô đã cung cấp các mẫu mô để George Otto Gey, người đứng đầu Phòng thí nghiệm Nuôi cấy Mô, đánh giá và nghiên cứu lâm sàng. Trợ lý phòng thí nghiệm của Gey, Mary Kubicek, đã sử dụng kỹ thuật ống lăn để đặt tế bào vào nuôi cấy.[9] Người ta quan sát thấy các tế bào phát triển mạnh mẽ, tăng gấp đôi sau mỗi 20–24 giờ, không giống như các mẫu vật trước đó đã chết.[11]
Các tế bào này được Gey nhân giống không lâu trước khi Lacks qua đời vì bệnh ung thư vào năm 1951. Đây là dòng tế bào đầu tiên của con người được chứng minh là nuôi cấy thành công trong ống nghiệm, đây là một thành tựu khoa học mang lại lợi ích sâu sắc cho nghiên cứu y học trong tương lai. Gey đã tặng miễn phí những tế bào này cùng với các công cụ và quy trình mà phòng thí nghiệm của ông đã phát triển cho bất kỳ nhà khoa học nào muốn nghiên cứu vì lợi ích của khoa học. Cả Lacks và gia đình cô đều chưa được xin phép để thu hoạch tế bào.[12] Các tế bào này sau đó đã được thương mại hóa, mặc dù chưa bao giờ được cấp bằng sáng chế ở dạng ban đầu. Vào thời điểm đó, không có yêu cầu phải thông báo cho bệnh nhân hoặc người thân của họ về những vấn đề đó vì các mẫu vật thải ra trong quá trình phẫu thuật, chẩn đoán hoặc điều trị là tài sản của bác sĩ hoặc cơ sở y tế.[cần dẫn nguồn]
Theo thông lệ đối với trợ lý phòng thí nghiệm của Gey, tế bào nuôi cấy được đặt tên tuân thủ theo hai chữ cái đầu tiên trong họ và tên của Henrietta Lacks, vì thế dòng tế bào này được gọi là HeLa.[9] Trước khi bị rò rỉ thông tin ra công chúng vào những năm 1970, tiết lộ tên thật của cô, dòng tế bào "HeLa" đã bị nhầm tưởng là được đặt theo tên của "Helen Lane" hoặc "Helen Larson".[6][13]
Các tế bào nuôi cấy khác đang bị các tế bào HeLa nghi ngờ xâm chiếm, vì vậy một nhóm nghiên cứu đã liên hệ với gia đình Lacks để tìm kiếm mẫu DNA nhằm giúp xác định các dòng tế bào gây ô nhiễm. Gia đình chưa bao giờ hiểu mục đích của chuyến thăm, nhưng họ rất đau khổ vì hiểu được những gì các nhà nghiên cứu đã nói với họ.[13][14] Những tế bào này được coi là tế bào ung thư, vì chúng có nguồn gốc từ sinh thiết lấy từ một tổn thương có thể nhìn thấy trên cổ tử cung như một phần trong chẩn đoán ung thư của Lacks.[15]
Tế bào HeLa, giống như các dòng tế bào khác, được gọi là "bất tử" ở chỗ chúng có thể phân chia không giới hạn số lần trong đĩa nuôi cấy tế bào trong phòng thí nghiệm miễn là đáp ứng các điều kiện sống sót cơ bản của tế bào (tức là được duy trì trong môi trường thích hợp). Có nhiều chủng tế bào HeLa khi chúng tiếp tục biến đổi trong môi trường nuôi cấy tế bào, nhưng tất cả các tế bào HeLa đều có nguồn gốc từ cùng các tế bào khối u được loại bỏ khỏi Lacks. Tổng số tế bào HeLa được nhân lên trong nuôi cấy tế bào vượt xa tổng số tế bào có trong cơ thể Henrietta Lacks.[16]
Tranh cãi
[sửa | sửa mã nguồn]
Trường hợp của Lacks là một trong nhiều ví dụ điển hình của thế kỷ XX về việc thiếu sự chấp thuận của bệnh nhân có hiểu biết trong y học khi cơ sở điều trị hoặc bác sĩ lấy đi từ cơ thể của họ một mẫu vật. Sự liên lạc giữa người hiến mô và bác sĩ hầu như không tồn tại – tế bào được lấy mà không có sự đồng ý của bệnh nhân và bệnh nhân không được cho biết tế bào sẽ được sử dụng để làm gì. Bệnh viện Johns Hopkins, nơi Lacks được điều trị và thu hoạch mô, là bệnh viện duy nhất ở khu vực Baltimore nơi bệnh nhân người Mỹ gốc Phi có thể được chăm sóc miễn phí. Những bệnh nhân được chăm sóc miễn phí từ khu vực tách biệt này của bệnh viện thường trở thành đối tượng nghiên cứu mà họ không hề hay biết.[17] Gia đình của Lacks cũng không có quyền truy cập vào hồ sơ bệnh nhân của cô và không có quyền quyết định ai sẽ nhận tế bào HeLa hoặc chúng sẽ được sử dụng vào mục đích gì. Ngoài ra, khi tế bào HeLa được phổ biến và sử dụng thường xuyên hơn trong cộng đồng khoa học, người thân của Lacks không nhận được lợi ích tài chính nào và tiếp tục sống với khả năng tiếp cận chăm sóc sức khỏe hạn chế.[13][18]
Vấn đề ai sở hữu các mẫu mô được lấy để nghiên cứu đã được đưa ra trong vụ kiện của Tối cao pháp viện California trong vụ Moore kiện Regents của Đại học California vào năm 1990. Tòa án đã phán quyết rằng mô và tế bào bị loại bỏ của một người không phải là tài sản của người đó và có thể được thương mại hóa.[19]
Trường hợp của Lacks đã ảnh hưởng đến việc thiết lập Quy tắc chung vào năm 1981. Quy tắc chung thực thi sự đồng ý bằng cách đảm bảo rằng các bác sĩ sẽ thông báo cho bệnh nhân nếu họ dự định sử dụng bất kỳ mẫu vật nào trên cơ thể của bệnh nhân trong nghiên cứu và cho họ lựa chọn tiết lộ chi tiết hay không. Các mô được kết nối với tên của người hiến tặng cũng được quản lý chặt chẽ theo quy tắc này và các mẫu không còn được đặt bằng tên viết tắt của người hiến tặng mà thay vào đó bằng mã số.[19] Để giải quyết thêm vấn đề về quyền riêng tư của bệnh nhân, Johns Hopkins đã thành lập một ủy ban chung với Viện Y tế Quốc gia và một số thành viên gia đình của Lacks để xác định xem ai có quyền truy cập vào bộ gen của Henrietta Lacks.[20]
Vào năm 2021, gia đình của Henrietta Lacks khởi đơn kiện để đòi các khoản thanh toán trong quá khứ và tương lai cho việc bán tế bào HeLa được cho là trái phép và được biết đến rộng rãi bởi Thermo Fisher Scientific.[21] Gia đình của Lacks đã thuê luật sư để đòi bồi thường từ hơn 100 công ty dược phẩm đã sử dụng và thu lợi từ t��� bào HeLa.[22] Việc giải quyết vụ kiện với Thermo Fisher Scientific được công bố vào tháng 8 năm 2023 với các điều khoản không được tiết lộ.[23] Sau thỏa thuận dàn xếp, có thông báo rằng gia đình Lacks đang kiện công ty Ultragenyx.[24]
Sử dụng trong nghiên cứu
[sửa | sửa mã nguồn]Tế bào HeLa là tế bào đầu tiên của con người được nhân bản thành công vào năm 1953 bởi Theodore Puck và Philip I. Marcus tại Đại học Colorado, Denver.[25] Kể từ thời điểm đó, tế bào HeLa đã "liên tục được sử dụng để nghiên cứu về bệnh ung thư, AIDS, tác động của bức xạ và các chất độc hại, lập bản đồ gen và vô số mục đích khoa học khác."[26] Theo tác giả Rebecca Skloot, đến năm 2009, "nhiều hơn 60.000 bài báo khoa học đã được xuất bản về nghiên cứu được thực hiện trên HeLa, và con số đó đang tăng lên đều đặn với tốc độ hơn 300 bài báo mỗi tháng."[19]
Xóa bỏ bệnh bại liệt
[sửa | sửa mã nguồn]
Tế bào HeLa được Jonas Salk sử dụng để thử nghiệm Vắc-xin bại liệt đầu tiên vào những năm 1950. Quan sát thấy chúng dễ bị nhiễm bệnh bại liệt, khiến các tế bào bị nhiễm bệnh chết.[3] Điều này khiến tế bào HeLa rất được ưa chuộng để thử nghiệm vắc xin bại liệt vì có thể dễ dàng thu được kết quả. Cần một lượng lớn tế bào HeLa để thử nghiệm vắc xin bại liệt của Salk, khiến Tổ chức Quốc gia về Bệnh bại liệt ở trẻ sơ sinh (NFIP) phải tìm một cơ sở có khả năng sản xuất hàng loạt tế bào HeLa.[27] Vào mùa xuân năm 1953, một nhà máy nuôi cấy tế bào được thành lập tại Đại học Tuskegee để cung cấp tế bào HeLa cho Salk và các phòng thí nghiệm khác.[28] Chưa đầy một năm sau, vắc xin của Salk đã sẵn sàng để thử nghiệm trên người.[29]
Virus học
[sửa | sửa mã nguồn]Tế bào HeLa đã được sử dụng để kiểm tra xem parvovirus lây nhiễm vào tế bào của người, chó và mèo như thế nào.[30] Những tế bào này cũng đã được sử dụng để nghiên cứu các loại virus như oropouche virus (OROV). OROV gây ra sự gián đoạn của các tế bào trong quá trình nuôi cấy, trong đó các tế bào bắt đầu thoái hóa ngay sau khi chúng bị nhiễm bệnh, gây ra hiện tượng virus chết tế bào theo chương trình.[31] Tế bào HeLa đã được sử dụng để nghiên cứu sự biểu hiện của papillomavirus E2 và apoptosis.[32] Tế bào HeLa cũng đã được sử dụng để nghiên cứu khả năng gây ra apoptosis của virus gây bệnh ở chó trong các dòng tế bào ung thư,[33] có thể đóng vai trò quan trọng trong việc phát triển các phương pháp điều trị cho các tế bào khối u kháng lại bức xạ và hóa trị.[33]
Tế bào HeLa cũng đóng vai trò quan trọng trong việc phát triển vắc xin ngừa Nhiễm virus papilloma ở người (HPV). Vào những năm 1980, Harald zur Hausen phát hiện ra rằng các tế bào của Lacks từ sinh thiết ban đầu có chứa HPV-18, loại vi rút này sau đó được phát hiện là nguyên nhân gây ra căn bệnh ung thư ác tính đã giết chết Henrietta Lacks. Công trình liên kết HPV với ung thư cổ tử cung của ông đã mang lại cho ông giải thưởng Nobel và dẫn đến sự phát triển các loại vắc xin HPV được dự đoán sẽ làm giảm 70% số ca tử vong do ung thư cổ tử cung.[34]
Trong những năm qua, các tế bào HeLa đã bị nhiễm nhiều loại vi-rút khác nhau bao gồm HIV, sốt rét, bệnh mụn rộp và quai bị để thử nghiệm và phát triển các loại vắc-xin và thuốc mới. Tiến sĩ Richard Axel phát hiện ra rằng bằng cách thêm protein CD4 vào tế bào HeLa, chúng có thể bị nhiễm HIV, cho phép nghiên cứu virus.[35] Năm 1979, các nhà khoa học biết được virus sởi liên tục biến đổi khi lây nhiễm vào tế bào HeLa[36] và vào năm 2019, họ phát hiện ra rằng vi rút sởi không thể nhân lên trong tế bào HeLa.[37]
Bệnh ung thư
[sửa | sửa mã nguồn]Tế bào HeLa đã được sử dụng trong một số nghiên cứu về ung thư, bao gồm cả những nghiên cứu liên quan đến hormone steroid sinh dục như estradiol, estrogen và thụ thể estrogen, cùng với các hợp chất giống estrogen như quercetin và đặc tính giảm ung thư của nó.[38] Cũng đã có nghiên cứu về tế bào HeLa, tác dụng của flavonoid và chất chống oxy hóa với estradiol đối với sự tăng sinh tế bào ung thư.
Vào năm 2011, tế bào HeLa đã được sử dụng trong các thử nghiệm thuốc nhuộm heptamethine mới IR-808 và các chất tương tự khác hiện đang được khám phá vì những ứng dụng độc đáo của chúng trong chẩn đoán y tế, phát triển liệu pháp trị liệu, điều trị cá nhân cho bệnh nhân ung thư với sự hỗ trợ của PDT, đồng thời-quản lý với các loại thuốc khác, và chiếu xạ.[39][40] Tế bào HeLa đã được sử dụng trong nghiên cứu liên quan đến fullerene để gây ra apoptosis như một phần của liệu pháp quang động, cũng như trong nghiên cứu ung thư trong ống nghiệm sử dụng các dòng tế bào.[41] Các tế bào HeLa khác cũng đã được sử dụng để xác định các dấu hiệu ung thư trong RNA và được sử dụng để thiết lập Hệ thống nhận dạng dựa trên RNAi và sự can thiệp của các tế bào ung thư cụ thể.[42]
HeLa đã được chứng minh vào năm 2014 là dòng tế bào khả thi để ghép xenograft khối u ở chuột trụi C57BL/6,[43] và sau đó được sử dụng để kiểm tra tác dụng in vivo của fluoxetine và cisplatin đối với ung thư cổ tử cung.
Di truyền học
[sửa | sửa mã nguồn]Năm 1953, một lỗi trong phòng thí nghiệm liên quan đến việc trộn nhầm tế bào HeLa với chất lỏng sai đã cho phép các nhà nghiên cứu nhìn và đếm rõ ràng từng nhiễm sắc thể trong tế bào HeLa mà họ đang làm việc cùng lần đầu tiên. Phát hiện tình cờ này đã khiến các nhà khoa học Joe Hin Tjio và Albert Levan phát triển các kỹ thuật nhuộm và đếm nhiễm sắc thể tốt hơn.[34] Họ là những người đầu tiên mô tả chính xác rằng con người có 23 cặp nhiễm sắc thể thay vì 24 như người ta tin trước đây. Điều này rất quan trọng đối với việc nghiên cứu các rối loạn phát triển như hội chứng Down liên quan đến số lượng nhiễm sắc thể.
Năm 1965, Henry Harris và John Watkins đã tạo ra giống lai giữa người và động vật đầu tiên bằng cách kết hợp tế bào HeLa với tế bào phôi chuột. Điều này cho phép tiến bộ trong việc lập bản đồ gen tới các nhiễm sắc thể cụ thể, cuối cùng dẫn đến Dự án Bộ gen Người.[34]
Vi sinh vật không gian
[sửa | sửa mã nguồn]Vào những năm 1960, tế bào HeLa đã được gửi lên vệ tinh Sputnik-6 của Liên Xô và các sứ mệnh không gian của con người để xác định tác động lâu dài của việc du hành vũ trụ lên tế bào và mô sống. Các nhà khoa học phát hiện ra rằng tế bào HeLa thậm chí còn phân chia nhanh hơn trong môi trường không trọng lực.[44]
Phân tích
[sửa | sửa mã nguồn]Telomerase
[sửa | sửa mã nguồn]Dòng tế bào HeLa được tạo ra để sử dụng trong nghiên cứu ung thư. Những tế bào này sinh sôi nảy nở nhanh chóng một cách bất thường, thậm chí so với các tế bào ung thư khác. Giống như nhiều tế bào ung thư khác,[45] tế bào HeLa có phiên bản hoạt động của telomerase trong quá trình phân chia tế bào,[46] sao chép telomere nhiều lần. Điều này ngăn chặn sự rút ngắn ngày càng tăng của telomere có liên quan đến lão hóa và cuối cùng là chết tế bào. Bằng cách này, các tế bào sẽ phá vỡ giới hạn Hayflick, đó là số lần phân chia tế bào giới hạn mà hầu hết các tế bào bình thường có thể trải qua trước khi trở thành lão hóa. Kết quả là sự phân chia tế bào không giới hạn và sự bất tử.
Số nhiễm sắc thể
[sửa | sửa mã nguồn]Việc chuyển gen ngang từ papillomavirus 18 (HPV18) ở người sang tế bào cổ tử cung của con người đã tạo ra bộ gen HeLa, khác với bộ gen của Henrietta Lacks về nhiều mặt, bao gồm cả số lượng nhiễm sắc thể. Tế bào HeLa là tế bào ung thư phân chia nhanh chóng và số lượng nhiễm sắc thể thay đổi trong quá trình hình thành ung thư và nuôi cấy tế bào. Ước tính hiện tại (không bao gồm các đoạn rất nhỏ) là "số lượng nhiễm sắc thể siêu tam bội (3n+)" có nghĩa là tổng số 76 đến 80 nhiễm sắc thể (chứ không phải số lượng lưỡng bội bình thường là 46) với 22–25 nhiễm sắc thể bất thường về dòng vô tính, được gọi là "nhiễm sắc thể đặc trưng HeLa".[47][48][49][50] Các nhiễm sắc thể đặc trưng có thể được lấy từ nhiều nhiễm sắc thể ban đầu, tạo ra số lượng tóm tắt đầy thách thức dựa trên cách đánh số ban đầu. Các nhà nghiên cứu cũng đã lưu ý rằng những kiểu nhân bất thường này có thể ổn định đến mức nào.[47] Các nghiên cứu kết hợp phương pháp phân tích nhiễm sắc thể quang phổ, FISH và các kỹ thuật tế bào học thông thường cho thấy những sai lệch nhiễm sắc thể được phát hiện có thể là đại diện của ung thư biểu mô cổ tử cung tiến triển và có thể đã hiện diện trong khối u nguyên phát, vì bộ gen HeLa vẫn ổn định ngay cả sau nhiều năm tiếp tục nuôi cấy.[47]
Trình tự bộ gen hoàn chỉnh
[sửa | sửa mã nguồn]Bộ gen hoàn chỉnh của tế bào HeLa đã được giải trình tự và công bố vào ngày 11 tháng 3 năm 2013[51][52] mà gia đình Lacks không hề hay biết.[53] Gia đình đã nêu lên mối lo ngại nên các tác giả đã tự nguyện từ chối quyền truy cập vào dữ liệu trình tự.[53] Jay Shendure đã dẫn đầu một dự án giải trình tự HeLa tại Đại học Washington, dự án này đã tạo ra một bài báo khoa học đã được chấp nhận xuất bản vào tháng 3 năm 2013 – nhưng bài báo đó cũng bị hoãn lại trong khi những lo ngại về quyền riêng tư của gia đình Lacks đang được giải quyết.[54] Vào ngày 7 tháng 8 năm 2013, giám đốc Viện Y tế Quốc gia là Francis Collins đã công bố chính sách truy cập có kiểm soát vào bộ gen của dòng tế bào dựa trên thỏa thuận đạt được sau ba cuộc gặp với gia đình Lacks.[55] Một ủy ban truy cập dữ liệu sẽ xem xét các yêu cầu của các nhà nghiên cứu về quyền truy cập vào trình tự bộ gen theo tiêu chí nghiên cứu dành cho nghiên cứu y học và người dùng sẽ tuân thủ các điều khoản trong Thỏa thuận sử dụng dữ liệu bộ gen HeLa, trong đó bao gồm tất cả các nhà nghiên cứu do Viện Y tế Quốc gia tài trợ sẽ gửi dữ liệu vào một cơ sở dữ liệu duy nhất để chia sẻ trong tương lai. Ủy ban bao gồm 6 thành viên bao gồm các đại diện từ các lĩnh vực y tế, khoa học và đạo đức sinh học, cũng như hai thành viên của gia đình Lacks.[53] Trong một cuộc phỏng vấn, Collins ca ngợi sự sẵn lòng của gia đình Lacks khi tham gia vào tình huống bu��c họ phải gánh chịu này. Ông mô tả toàn bộ trải nghiệm với họ là "mạnh mẽ", nói rằng nó tập hợp "khoa học, lịch sử khoa học và các mối quan tâm về đạo đức" theo một cách độc đáo.[56]
Sự ô nhiễm
[sửa | sửa mã nguồn]Tế bào HeLa đôi khi khó kiểm soát vì chúng thích nghi với sự phát triển trong đĩa nuôi cấy mô với khả năng xâm lấn và cạnh tranh với các dòng tế bào khác. Thông qua việc bảo trì không đúng cách, chúng đã làm ô nhiễm các tế bào nuôi cấy khác trong cùng phòng thí nghiệm, cản trở nghiên cứu sinh học và buộc các nhà nghiên cứu phải tuyên bố nhiều kết quả không đúng. Mức độ ô nhiễm tế bào HeLa giữa các loại tế bào khác vẫn chưa được biết rõ vì rất ít nhà nghiên cứu kiểm tra danh tính hoặc độ tinh khiết của các dòng tế bào đã được thiết lập. Người ta đã chứng minh rằng một phần đáng kể các dòng tế bào in vitro bị nhiễm tế bào HeLa; ước tính dao động từ 10% đến 20%. Quan sát này cho thấy rằng bất kỳ dòng tế bào nào cũng có thể dễ bị nhiễm bẩn ở một mức độ nào đó. Stanley Michael Gartler (1967) và Walter Nelson-Rees (1975) là những người đầu tiên công bố về sự lây nhiễm của các dòng tế bào khác nhau bởi HeLa.[27] Gartler lưu ý rằng "Với sự mở rộng liên tục của công nghệ nuôi cấy tế bào, gần như chắc chắn rằng cả ô nhiễm giữa các loài và trong cùng loài sẽ xảy ra."[9]
Ô nhiễm tế bào HeLa đã trở thành một vấn đề phổ biến trên toàn thế giới - ảnh hưởng đến cả phòng thí nghiệm của nhiều bác sĩ, nhà khoa học và nhà nghiên cứu nổi tiếng, bao gồm cả Jonas Salk. Vấn đề ô nhiễm HeLa cũng góp phần gây ra căng thẳng trong Chiến tranh Lạnh. Liên Xô và Hoa Kỳ đã bắt đầu hợp tác trong cuộc chiến chống ung thư do Tổng thống Richard Nixon phát động, chỉ để phát hiện ra rằng các tế bào được trao đổi đã bị nhiễm HeLa.[57]
Thay vì tập trung vào cách giải quyết vấn đề ô nhiễm tế bào HeLa, nhiều nhà khoa học và tác giả khoa học tiếp tục ghi nhận vấn đề này đơn giản là vấn đề ô nhiễm - không phải do lỗi hoặc thiếu sót của con người mà do bản chất cứng rắn, sinh sôi nảy nở quá mạnh của HeLa.[58] Dữ liệu gần đây cho thấy ô nhiễm chéo vẫn là một vấn đề lớn đang diễn ra với nuôi cấy tế bào hiện đại.[5][59] Ủy ban Xác thực Dòng Tế bào Quốc tế (ICLAC) lưu ý rằng nhiều trường hợp xác định sai dòng tế bào là kết quả của sự lây nhiễm chéo môi trường nuôi cấy bởi một dòng tế bào phát triển nhanh hơn khác. Điều này đặt ra câu hỏi về giá trị của nghiên cứu được thực hiện bằng cách sử dụng các dòng tế bào bị ô nhiễm, vì một số thuộc tính nhất định của chất gây ô nhiễm, có thể đến từ một loài hoặc mô hoàn toàn khác, có thể được phân bổ sai cho dòng tế bào đang được điều tra.[60]
Đề xuất loài mới
[sửa | sửa mã nguồn]
HeLa được nhà sinh vật học tiến hóa Leigh Van Valen mô tả như một ví dụ về việc tạo ra một loài mới đương thời, được đặt tên là "Helacyton gartleri", do khả năng sao chép vô thời hạn và số lượng nhiễm sắc thể không phải của con người. Loài này được đặt theo tên của nhà di truyền học Stanley Michael Gartler, người mà Van Valen cho rằng đã khám phá ra "sự thành công đáng chú ý của loài này".[61] Lập luận của ông về sự hình thành loài phụ thuộc vào những điểm sau:
- Sự không tương thích nhiễm sắc thể của tế bào HeLa với con người.
- Ổ sinh thái của tế bào HeLa.
- Khả năng tồn tại và phát triển của chúng vượt xa mong muốn của người nuôi cấy.
- HeLa có thể được định nghĩa là một loài vì nó có kiểu nhân đồ riêng.[62]
Van Valen đề xuất họ mới là Helacytidae và chi Helacyton, cũng như đề xuất một loài mới cho tế bào HeLa trong cùng một bài báo.[63]
Tuy nhiên, đề xuất này chưa được các nhà sinh học tiến hóa nổi tiếng khác cũng như các nhà khoa học thuộc các ngành khác coi trọng. Lập luận của Van Valen về việc HeLa là một loài mới không đáp ứng các tiêu chí cho một loài sinh sản vô tính đơn bào độc lập vì sự bất ổn của kiểu nhân của HeLa và việc chúng thiếu một dòng dõi tổ tiên nghiêm ngặt.[64]
Hình ảnh
[sửa | sửa mã nguồn]-
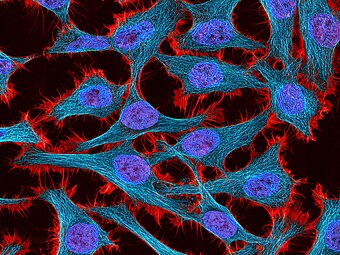
Hình ảnh huỳnh quang đa photon của các tế bào HeLa được nhuộm bằng phalloidin độc tố liên kết Actin (màu đỏ), vi ống (màu lục lam) và nhân tế bào (màu xanh). Kính hiển vi quét laser tùy chỉnh Nikon RTS2000MP.
-
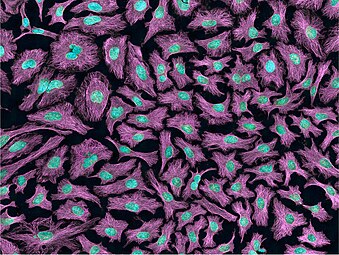
Hình ảnh huỳnh quang đa photon của tế bào HeLa với các vi ống tế bào (màu đỏ tươi) và DNA (màu lục lam). Kính hiển vi quét laser tùy chỉnh Nikon RTS2000MP..
-
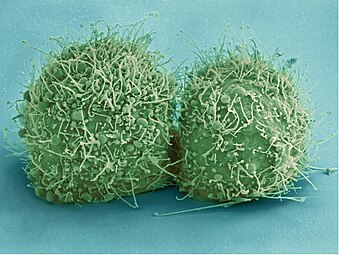
Ảnh hiển vi điện tử quét của các tế bào HeLa vừa phân chia. Zeiss Merlin HR-SEM.
-
Các tế bào HeLa được nhuộm bằng Hoechst 33258
-
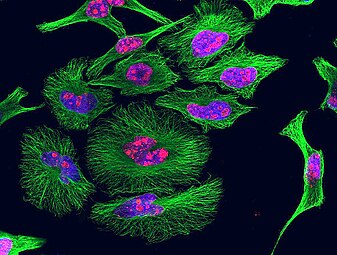
Các tế bào HeLa được nuôi cấy và nhuộm màu bằng kháng thể kháng tubulin (màu xanh lá cây), kháng thể kháng Ki-67 (màu đỏ) và thuốc nhuộm liên kết DNA màu xanh lam DAPI. Kháng thể tubulin thể hiện sự phân bố của vi ống và kháng thể Ki-67 được biểu hiện trong các tế bào sắp phân chia. Sự chuẩn bị, kháng thể và hình ảnh được cung cấp bởi EnCor Biotechnology.
-
Một bề mặt thể tích hiển thị (màu đỏ) của Màng nhân của một tế bào HeLa. Tế bào được quan sát trong 300 lát kính hiển vi điện tử, lớp vỏ hạt nhân được tự động phân đoạn và hiển thị. Một lát dọc và một lát ngang được thêm vào để tham khảo.
-
Màng plasma và vỏ bọc hạt nhân của một tế bào Hela được hiển thị dưới dạng hiển thị bề mặt thể tích. Bên trái và giữa hiển thị màng plasma có màu xanh lam trong suốt và lớp vỏ hạt nhân có màu lục lam đậm. Bên phải hiển thị màng plasma không có độ trong suốt và góc nhìn giống như trung tâm. Các màng này đã được phân đoạn từ dữ liệu thu được bằng Kính hiển vi điện tử.
Trong phương tiện truyền thông
[sửa | sửa mã nguồn]- Bộ phim tài liệu "The Way of All Flesh" năm 1997 của Adam Curtis giải thích lịch sử của HeLa và ý nghĩa của nó trong y học và xã hội.[65]
- Một tập phim Law & Order "Immortal" năm 2010 dựa chủ yếu vào câu chuyện của Henrietta Lacks và dòng HeLa, sử dụng các tế bào "NaRo" hư cấu làm thế thân.[66]
- Câu chuyện về sự ra đời của dòng HeLa cũng là chủ đề của một tập podcast Radiolab năm 2010.[67]
- HeLa là chủ đề trong cuốn sách xuất bản năm 2010 của Rebecca Skloot, Cuộc đời bất tử của Henrietta Lacks, điều tra bối cảnh lịch sử của dòng tế bào và cách gia đình Lacks tham gia vào việc sử dụng nó.[13]
- Một bộ phim HBO năm 2017, Cuộc đời bất tử của Henrietta Lacks (phim) dựa trên cuốn sách cùng tên. Phim có sự tham gia của Oprah Winfrey, Sylvia Grace Crim, Rocky Carroll và Renée Elise Goldsberry trong vai Henrietta Lacks. Tác giả Rebecca Skloot cũng xuất hiện với tư cách là một nhân vật trong phim do Rose Byrne thể hiện.[68]
Tham khảo
[sửa | sửa mã nguồn]- ^ Rahbari R, Sheahan T, Modes V, Collier P, Macfarlane C, Badge RM (2009). “A novel L1 retrotransposon marker for HeLa cell line identification”. BioTechniques. 46 (4): 277–284. doi:10.2144/000113089. PMC 2696096. PMID 19450234.
- ^ Morris, Rhys Bowen (2 tháng 8 năm 2023). “What were the top 100 cell lines of 2022?”. CiteAb Blog (bằng tiếng Anh). Truy cập ngày 17 tháng 8 năm 2023.
- ^ a b Scherer, W.F.; Syverton, J.T.; Gey, G.O. (1953). “Studies on the propagation in vitro of poliomyelitis viruses. IV. Viral multiplication in a stable strain of human malignant epithelial cells (strain HeLa) derived from an epidermoid carcinoma of the cervix”. Journal of Experimental Medicine. 97 (5): 695–710. doi:10.1084/jem.97.5.695. PMC 2136303. PMID 13052828.
- ^ “Johns Hopkins Magazine -- April 2000”. pages.jh.edu.
- ^ a b Capes-Davis A, Theodosopoulos G, Atkin I, Drexler HG, Kohara A, MacLeod RA, Masters JR, Nakamura Y, Reid YA, Reddel RR, Freshney RI (2010). “Check your cultures! A list of cross-contaminated or misidentified cell lines”. Int. J. Cancer. 127 (1): 1–8. doi:10.1002/ijc.25242. PMID 20143388. S2CID 2929020.
- ^ a b Batts DW (10 tháng 5 năm 2010). “Cancer cells killed Henrietta Lacks – then made her immortal”. The Virginian-Pilot. tr. 1, 12–14. Bản gốc lưu trữ ngày 25 tháng 11 năm 2016. Truy cập ngày 8 tháng 5 năm 2020.
- ^ Ron Claiborne; Sydney Wright, IV (31 tháng 1 năm 2010). “How One Woman's Cells Changed Medicine”. ABC World News. Truy cập ngày 19 tháng 8 năm 2012.
- ^ McKie, Robin (3 tháng 4 năm 2010). “Henrietta Lacks's cells were priceless, but her family can't afford a hospital”. The Guardian. London. Truy cập ngày 18 tháng 7 năm 2017.
- ^ a b c d Lucey, Brendan P.; Nelson-Rees, Walter A.; Hutchins, Grover M. (21 tháng 10 năm 2009). “Henrietta Lacks, HeLa Cells, and Cell Culture Contamination”. Archives of Pathology & Laboratory Medicine (bằng tiếng Anh). 133 (9): 1463–7. doi:10.5858/133.9.1463. PMID 19722756.
- ^ Jones, Howard W. (1 tháng 6 năm 1997). “Record of the first physician to see Henrietta Lacks at the Johns Hopkins Hospital: History of the beginning of the HeLa cell line”. American Journal of Obstetrics and Gynecology (bằng tiếng Anh). 176 (6): s227–s228. doi:10.1016/S0002-9378(97)70379-X. ISSN 0002-9378. PMID 9215212.
- ^ Butanis, Benjamin. “The Legacy of Henrietta Lacks”. www.hopkinsmedicine.org (bằng tiếng Anh). Truy cập ngày 7 tháng 5 năm 2020.
- ^ Washington, Harriet "Henrietta Lacks: An Unsung Hero", Emerge Magazine, October 1994
- ^ a b c d Zielinski, Sarah (2 tháng 1 năm 2010). “Cracking the code of the human genome – Henrietta Lacks' 'immortal' cells”. Smithsonian. Truy cập ngày 27 tháng 5 năm 2017.
- ^ White, Tracie (2 tháng 5 năm 2018), “Descendants of Henrietta Lacks discuss her famous cell line”, Stanford Medicine News Center, truy cập ngày 9 tháng 12 năm 2021
- ^ del Carpio, Alexandra (27 tháng 4 năm 2014). “The Good, the Bad, and the HeLa”. Berkeley Science Review. Bản gốc lưu trữ ngày 23 tháng 5 năm 2017. Truy cập ngày 27 tháng 5 năm 2017.
- ^ Sharrer T (2006). “"HeLa" Herself”. The Scientist. 20 (7): 22.
- ^ Stump, Jessica L. (2014). “Henrietta Lacks and The HeLa Cell: Rights of Patients and Responsibilities of Medical Researchers”. The History Teacher. 48 (1): 127–180. ISSN 0018-2745. JSTOR 43264385.
- ^ Day, Jo Ann. “Upholding the Highest Bioethical Standards | Johns Hopkins Medicine”. www.hopkinsmedicine.org (bằng tiếng Anh). Truy cập ngày 15 tháng 4 năm 2020.
- ^ a b c Skloot, Rebecca (2010). The Immortal Life of Henrietta Lacks. New York: Crown/Random House. ISBN 978-1-4000-5217-2.
- ^ “HeLa Cell Line Origins, Contamination, Controversy, and Cytogenetics” (bằng tiếng Anh). Truy cập ngày 15 tháng 4 năm 2020.
- ^ “Estate of Henrietta Lacks sues Thermo Fisher over the improper sale of her immortal cells”.
- ^ “Family of Henrietta Lacks hires civil rights attorney to seek funds over famous cells”. Washington Post (bằng tiếng Anh). ISSN 0190-8286. Truy cập ngày 11 tháng 12 năm 2021.
- ^ Holpuch, Amanda (1 tháng 8 năm 2023). “Family of Henrietta Lacks Settles With Biotech Company That Used Her Cells”. The New York Times.
- ^ “Ultragenyx Sued by Henrietta Lacks' Family in Second HeLa Cell Line Lawsuit” (bằng tiếng Anh). Truy cập ngày 11 tháng 8 năm 2023.
- ^ Puck, T.T.; Marcus, P.I. (1955). “A rapid method for viable cell titration and clone production with Hela cells in tissue culture: The use of X-irradiated cells to supply conditioning factors”. Proceedings of the National Academy of Sciences of the United States of America (xuất bản 15 tháng 7 năm 1955). 41 (7): 432–437. Bibcode:1955PNAS...41..432P. doi:10.1073/pnas.41.7.432. PMC 528114. PMID 16589695.
- ^ Smith, Van (17 tháng 4 năm 2002). “Wonder Woman: The Life, Death, and Life After Death of Henrietta Lacks, Unwitting Heroine of Modern Medical Science”. Baltimore City Paper. Bản gốc lưu trữ ngày 14 tháng 8 năm 2004. Truy cập ngày 2 tháng 3 năm 2017.
- ^ a b Masters, John R. (2002). “HeLa cells 50 years on: The good, the bad and the ugly”. Nature Reviews Cancer. 2 (4): 315–319. doi:10.1038/nrc775. PMID 12001993. S2CID 991019.
- ^ Turner, Timothy (2012). “Development of the Polio Vaccine: A Historical Perspective of Tuskegee University's Role in Mass Production and Distribution of HeLa Cells”. Journal of Health Care for the Poor and Underserved. 23 (4a): 5–10. doi:10.1353/hpu.2012.0151. PMC 4458465. PMID 23124495.
- ^ Brownlee, K. A. (1955). “Statistics of the 1954 Polio Vaccine Trials*”. Journal of the American Statistical Association. 50 (272): 1005–1013. doi:10.1080/01621459.1955.10501286.
- ^ Parker, J; Murphy W; Wang D; O'Brien S; Parrish C (2001). “Canine and feline parvoviruses can use human or feline transferrin receptors to bind, enter, and infect cells”. Journal of Virology. 75 (8): 3896–3902. doi:10.1128/JVI.75.8.3896-3902.2001. PMC 114880. PMID 11264378.
- ^ Acrani, G.O.; Gomes, R.; Proença-Módena, J.L.; da Silva, A.F.; Carminati, P.O.; Silva, M.L.; Santos, R.I.; Arruda, E. (2010). “Apoptosis induced by Oropouche virus infection in HeLa cells is dependent on virus protein expression”. Virus Research. 149 (1): 56–63. doi:10.1016/j.virusres.2009.12.013. PMID 20080135.
- ^ Hou, S.Y.; Wu, S.; Chiang, C. (2002). “Transcriptional activity among high and low risk human papillomavirus E2 proteins correlates with E2 DNA binding”. The Journal of Biological Chemistry. 277 (47): 45619–45629. doi:10.1074/jbc.M206829200. PMID 12239214. S2CID 9203953.
- ^ a b del Puerto, H.L.; Martins, A.S.; Milsted, A.; Souza-Fagundes, E.M.; Braz, G.F.; Hissa, B.; Andrade, L.O.; Alves, F.; Rajão, D.S.; Leite, R.C.; Vasconcelos, A.C. (2011). “Canine distemper virus induces apoptosis in cervical tumor derived cell lines”. Virol. J. 8 (1): 334. doi:10.1186/1743-422X-8-334. PMC 3141686. PMID 21718481.
- ^ a b c “5 Contributions HeLa Cells Have Made to Science”. Cell Science from Technology Networks (bằng tiếng Anh). Truy cập ngày 25 tháng 3 năm 2020.
- ^ Mondor, Isabelle; Ugolini, Sophie; Sattentau, Quentin J. (1 tháng 5 năm 1998). “Human Immunodeficiency Virus Type 1 Attachment to HeLa CD4 Cells Is CD4 Independent and gp120 Dependent and Requires Cell Surface Heparans”. Journal of Virology. 72 (5): 3623–3634. doi:10.1128/jvi.72.5.3623-3634.1998. ISSN 1098-5514. PMC 109583. PMID 9557643.
- ^ Wechsler, Steven L.; Rustigian, Robert; Stallcup, Kathryn C.; Byers, Karen B.; Winston, Stuart H.; Fields, Bernard N. (1979). “Measles Virus-Specified Polypeptide Synthesis in Two Persistently Infected HeLa Cell Lines”. Journal of Virology. 31 (3): 677–684. doi:10.1128/jvi.31.3.677-684.1979. ISSN 0022-538X. PMC 353496. PMID 513191.
- ^ Li, Li; Collins, Natalie D.; Widen, Steven G.; Davis, Emily H.; Kaiser, Jaclyn A.; White, Mellodee M.; Greenberg, M. Banks; Barrett, Alan D. T.; Bourne, Nigel; Sarathy, Vanessa V. (20 tháng 8 năm 2019). “Attenuation of Zika Virus by Passage in Human HeLa Cells”. Vaccines. 7 (3): 93. doi:10.3390/vaccines7030093. ISSN 2076-393X. PMC 6789458. PMID 31434319.
- ^ Pamela Bulzomi; Paola Galluzzo; Alessandro Bolli; Stefano Leone; Filippo Acconcia; Maria Marino (2012). “The pro-apoptotic effect of quercetin in cancer cell lines requires ERβ-dependent signals”. Journal of Cellular Physiology. 227 (5): 1891–1898. doi:10.1002/jcp.22917. PMID 21732360. S2CID 24034074.
- ^ Tan X, Luo S, Wang D, Su Y, Cheng T, Shi C (2011). “A NIR heptamethine Dye with intrinsic cancer targeting, imaging and photosynthesizing properties”. Journal of Biomaterials China. 33 (7): 2230–2239. doi:10.1016/j.biomaterials.2011.11.081. PMID 22182749.
- ^ Pene, F.; Courtine, E.; Cariou, A.; Mira, J.P. (2009). “Toward theranostics”. Crit Care Med. 37 (1 Suppl): S50–S58. doi:10.1097/CCM.0b013e3181921349. PMID 19104225. S2CID 37043095.
- ^ Briiuner., Thomas; Dieter F. Hulser (1990). “Tumor Cell Invasion and Gap Junctional Communication” (PDF). Invasion Metastasis. 10: 31–34. Truy cập ngày 3 tháng 4 năm 2012.
- ^ Xie, Z.; Wroblewska, L.; Prochazka, L.; Weiss, R.; Benenson, Y. (2011). “Multi-Input RNAi-Based Logic Circuit for Identification of Specific Cancer Cells” (PDF). Science. 333 (6047): 1307–1311. Bibcode:2011Sci...333.1307X. doi:10.1126/science.1205527. PMID 21885784. S2CID 13743291.
- ^ Arjomandnejad, M; và đồng nghiệp (2014). “HeLa cell line xenograft tumor as a suitable cervical cancer model: growth kinetic characterization and immunohistochemistry array” (PDF). Archives of Iranian Medicine. 17 (4): 273–277. PMID 24724604. S2CID 25652255. Bản gốc (PDF) lưu trữ ngày 25 tháng 4 năm 2018.
- ^ Davies, Preston. “Significant Research Advances Enabled by HeLa Cells”. Office of Science Policy (bằng tiếng Anh). Bản gốc lưu trữ ngày 2 tháng 2 năm 2020. Truy cập ngày 25 tháng 3 năm 2020.
- ^ The Nobel Prize in Physiology or Medicine 2009 on nobelprize.org
- ^ Ivanković M, Cukusić A, Gotić I, Skrobot N, Matijasić M, Polancec D, Rubelj I (2007). “Telomerase activity in HeLa cervical carcinoma cell line proliferation”. Biogerontology. 8 (2): 163–72. doi:10.1007/s10522-006-9043-9. PMID 16955216. S2CID 9390790.
- ^ a b c Macville M, Schröck E, Padilla-Nash H, Keck C, Ghadimi BM, Zimonjic D, Popescu N, Ried T (1999). “Comprehensive and definitive molecular cytogenetic characterization of HeLa cells by spectral karyotyping”. Cancer Res. 59 (1): 141–50. PMID 9892199.
- ^ Landry JJ, Pyl PT, Rausch T, Zichner T, Tekkedil MM, Stütz AM, Jauch A, Aiyar RS, Pau G, Delhomme N, Gagneur J, Korbel JO, Huber W, Steinmetz LM (2013). “The genomic and transcriptomic landscape of a HeLa cell line”. G3: Genes, Genomes, Genetics. 3 (8): 1213–24. doi:10.1534/g3.113.005777. PMC 3737162. PMID 23550136.
- ^ Bottomley, R.H.; Trainer, A.L.; Griffin, M.J. (1969). “Enzymatic and chromosomal characterization of HeLa variants”. J. Cell Biol. 41 (3): 806–15. doi:10.1083/jcb.41.3.806. PMC 2107821. PMID 5768876.
- ^ Andrew Adey; Joshua N. Burton; Jacob O. Kitzman; Joseph B. Hiatt; Alexandra P. Lewis; Beth K. Martin; Ruolan Qiu; Choli Lee; Jay Shendure (2013). “The haplotype-resolved genome and epigenome of the aneuploid HeLa cancer cell line”. Nature (xuất bản 8 tháng 8 năm 2013). 500 (7461): 207–211. Bibcode:2013Natur.500..207A. doi:10.1038/nature12064. PMC 3740412. PMID 23925245.
- ^ Landry JJ, Pyl PT, Rausch T, Zichner T, Tekkedil MM, Stütz AM, Jauch A, Aiyar RS, Pau G, Delhomme N, Gagneur J, Korbel JO, Huber W, Steinmetz LM (2013). “The genomic and transcriptomic landscape of a HeLa cell line”. G3: Genes, Genomes, Genetics. 3 (8): 1213–24. doi:10.1534/g3.113.005777. PMC 3737162. PMID 23550136.
- ^ Callaway, Ewen (15 tháng 3 năm 2013). “Most popular human cell in science gets sequenced”. Nature. doi:10.1038/nature.2013.12609. S2CID 87549985. Truy cập ngày 8 tháng 8 năm 2013.
- ^ a b c Callaway, Ewen (27 tháng 3 năm 2013). “HeLa publication brews bioethical storm”. Nature. doi:10.1038/nature.2013.12689. S2CID 88020977. Truy cập ngày 8 tháng 8 năm 2013.
- ^ Callaway, Ewen (7 tháng 8 năm 2013). “Deal done over HeLa cell line”. Nature. 500 (7461): 132–133. Bibcode:2013Natur.500..132C. doi:10.1038/500132a. PMID 23925220.
- ^ “NIH, Lacks family reach understanding to share genomic data of HeLa cells”. The National Institutes of Health. 7 tháng 8 năm 2013. Bản gốc lưu trữ ngày 11 tháng 8 năm 2013. Truy cập ngày 8 tháng 8 năm 2013.
- ^ Callaway, Ewen (7 tháng 8 năm 2013). “NIH director explains HeLa agreement”. Nature. doi:10.1038/nature.2013.13521. S2CID 190871214.
- ^ Gold, Michael (1986). A conspiracy of cells: one woman's immortal legacy and the medical scandal it caused. State University of New York Press. ISBN 0-88706-099-4. OCLC 12805138.
- ^ Wang H, Huang S, Shou J, Su EW, Onyia JE, Liao B, Li S (2006). “Comparative analysis and integrative classification of NCI60 cell lines and primary tumors using gene expression profiling data”. BMC Genomics. 7 (1): 166. doi:10.1186/1471-2164-7-166. PMC 1525183. PMID 16817967.
- ^ Nardone, R.M. (2007). “Eradication of cross-contaminated cell lines: A call for action” (PDF). Cell Biology and Toxicology. 23 (6): 367–372. CiteSeerX 10.1.1.432.8581. doi:10.1007/s10565-007-9019-9. PMID 17522957. S2CID 21077969. Bản gốc (PDF) lưu trữ ngày 17 tháng 12 năm 2008. Truy cập ngày 4 tháng 12 năm 2007.
- ^ “ATCC® Standards Development Organization: The International Cell Line Authentication Committee (ICLAC)”. Standards.atcc.org. Bản gốc lưu trữ ngày 8 tháng 5 năm 2013. Truy cập ngày 27 tháng 6 năm 2013.
- ^ Maiorana VC, Van Valen LM (7 tháng 2 năm 1991). “Hela, a new microbial species” (PDF). Evolutionary Theory (bằng tiếng Anh). 10 (2): 71–4. Lưu trữ (PDF) bản gốc ngày 29 tháng 3 năm 2018.
- ^ Duesberg, P; Mandrioli, D; McCormack, A; Nicholson, JM (2011). “Is carcinogenesis a form of speciation?”. Cell Cycle. Georgetown, Texas. 10 (13): 2100–2114. doi:10.4161/cc.10.13.16352. PMID 21666415.
- ^ van Valen, L.M.; Maiorana, V.C. (1991). “HeLa, a new microbial species”. Evolutionary Theory & Review. 10: 71–74. ISSN 1528-2619.
- ^ Cohan, FM (2002). “What are bacterial species?”. Annu. Rev. Microbiol. 56 (1): 457–487. doi:10.1146/annurev.micro.56.012302.160634. PMID 12142474.
- ^ “Modern Times: The Way of All Flesh - BBC Two England - 19 March 1997”. The Radio Times (3815): 92. 13 tháng 3 năm 1997.
- ^ Thomas, June (19 tháng 5 năm 2010). “Ripped From Which Headline? "Immortal"”. Slate Magazine (bằng tiếng Anh). Truy cập ngày 3 tháng 8 năm 2021.
- ^ “Henrietta's Tumor”.
- ^ “About The Immortal Life of Henrietta Lacks”. Rebecca Skloot. Truy cập ngày 24 tháng 4 năm 2018.
Đọc thêm
[sửa | sửa mã nguồn]- Hannah Landecker (2000). “Immortality, In Vitro: A History of the HeLa Cell Line”. Trong Brodwin, Paul (biên tập). Biotechnology and culture: bodies, anxieties, ethics. Bloomington: Indiana University Press. tr. 53–74. ISBN 978-0-253-21428-7.
- Rebecca Skloot (2010). The Immortal Life of Henrietta Lacks.
Liên kết ngoài
[sửa | sửa mã nguồn]- HeLa (CCL-2 Cells) in the ATCC database
- MeSH HeLa Cells
- HeLa Transfection and Selection Data for HeLa Cells
- Rebecca Skloot, The Immortal Life of Henrietta Lacks book website with additional features (photo/video/audio)
- The Henrietta Lacks Foundation, a foundation established to, among other things, help provide scholarship funds and health insurance to Henrietta Lacks's family.
- Rebecca Skloot, Cells That Save Lives are a Mother's Legacy, New York Times
- "Wonder Woman: The Life, Death, and Life After Death of Henrietta Lacks, Unwitting Heroine of Modern Medical Science" by Van Smith
- "What's Left of Henrietta Lacks?" by Anne Enright
- "Culturing Life: How Cells Became Technologies" a book by Hannah Landecker about HeLa and the history of tissue culture.
- Discussion about the taxonomic effect of creating the new taxon Helacyton.
- Cell Centered Database – HeLa cell
- Audio Interview with Rebecca Skloot about her book "The Immortal Life of Henrietta Lacks"
- Cellosaurus entry for HeLa
- The Legacy of Henrietta Lacks