డైబోరాన్
| |
| |
| పేర్లు | |
|---|---|
| IUPAC నామము
Diborane(6)
| |
| ఇతర పేర్లు
Boroethane
Boron hydride Diboron hexahydride | |
| గుర్తింపు విషయాలు | |
| సి.ఎ.ఎస్. సంఖ్య | [19287-45-7] |
| యూరోపియన్ కమిషన్ సంఖ్య | 242-940-6 |
| సి.హెచ్.ఇ.బి.ఐ | CHEBI:33590 |
| ఆర్.టి.ఇ.సి.యస్. సంఖ్య | HQ9275000 |
| SMILES | [BH2]1[H][BH2][H]1 |
| |
| ధర్మములు | |
| B2H6 | |
| మోలార్ ద్రవ్యరాశి | 27.67 g·mol−1 |
| స్వరూపం | Colorless gas |
| వాసన | repulsive and sweet |
| సాంద్రత | 1.216 g/L |
| ద్రవీభవన స్థానం | −164.85 °C (−264.73 °F; 108.30 K) |
| బాష్పీభవన స్థానం | −92.5 °C (−134.5 °F; 180.7 K) |
| Reacts[1] | |
| బాష్ప పీడనం | 39.5 atm (16.6°C)[1] |
| నిర్మాణం | |
కోఆర్డినేషన్ జ్యామితి
|
Tetrahedral (for boron) |
| see text | |
ద్విధృవ చలనం
|
0 D |
| ప్రమాదాలు | |
| ప్రధానమైన ప్రమాదాలు | highly flammable, reacts with water |
స్వయం జ్వలన
ఉష్ణోగ్రత |
38 °C (100 °F; 311 K) |
| విస్ఫోటక పరిమితులు | 0.8%-88%[1] |
| Lethal dose or concentration (LD, LC): | |
LC50 (median concentration)
|
40 ppm (rat, 4 hr) 29 ppm (mouse, 4 hr) 40-80 ppm (rat, 4 hr) 159-181 ppm (rat, 15 min)[2] |
LCLo (lowest published)
|
125 ppm (dog, 2 hr) 50 ppm (hamster, 8 hr)[2] |
| US health exposure limits (NIOSH): | |
PEL (Permissible)
|
TWA 0.1 ppm (0.1 mg/m3)[1] |
REL (Recommended)
|
TWA 0.1 ppm (0.1 mg/m3)[1] |
IDLH (Immediate danger)
|
15 ppm[1] |
| సంబంధిత సమ్మేళనాలు | |
| Related {{{label}}} | {{{value}}} |
Except where otherwise noted, data are given for materials in their standard state (at 25 °C [77 °F], 100 kPa). | |
| Infobox references | |
డైబోరాన్అనునది బోరాన్, హైడ్రోజన్ మూలకాలను కలిగిఉన్న ఒక అకర్బన రసాయన సమ్మేళనపదార్థం.ఈ రసాయన సంయోగపదార్థం యొక్క సంకేతపదం B2H6. రంగులేని, గది ఉష్ణోగ్రత వద్ద స్థిరమైన స్వభావం ఉన్న అప్రియమైన తీపి వాసన ఉన్న సంయోగ పదార్థం డైబోరాన్.డైబోరాన్ గాలిలో బాగా మిశ్రమం చెంది/మిళితమై విస్పోటకకారక మిశ్రమాన్ని ఏర్పరచును.గది ఉష్ణోగ్రతవద్ద, తడికల్గిన/తేమ ఉన్న గాలితో కలిసి తనకుతానుగా ఉన్నపళంగా (spontaneously) మండును. బోరోఇథెన్, బోరాన్హైడ్రేడ్, డైబోరాన్ హెక్సాహైడ్రైడ్ వంటివి దీనికి సమాంతరమైన ఇతర బోరాన్ సమ్మేళన పదార్థాలు.బోరాన్ సమ్మేళన పదార్థాలలో డైబోరాన్ వివిధ ప్రయోజనాలు కల్గిన ముఖ్యమైన సంయోగ పదార్థం.ఈ రసాయన పదార్థాన్ని ఉష్ణగ్రాహక/తాపచూషకం (endothermic) గా వర్గీకరించారు.
చరిత్ర
[మార్చు]డైబోరాన్ మొదటగా 19 శతాబ్దిలో మెటల్ బోరిడీస్ (metal borides) లను జలవిశ్లేషణ (hydrolysis) కావించడం ద్వారా ఉత్పత్తి చేసారు.కాని ఎప్పుడు ఈఈ పదార్థాన్ని పరిశీలించి, విశ్లేషించలేదు.912 నుండి1936 వరకు బోరాన్ హైడ్రైడ్రసాయన శాస్త్ర పరిశోధనకు ప్రథముడు మార్గదర్శి అయిన అల్ఫ్రేడ్ స్టాక్ (Alfred Stock) తన పరిశోధనలను కొనసాగించి అత్యంత చర్యయుతమైన, తరచుగా విష స్వభావ, హానికరమైన బోరాన్ హైడైడ్ లను సంశ్లేషణ చేయు పద్ధతులను ఆవిష్కరించాడు.డైబోరాన్ సౌష్టవం ఈథెన్ వంటి నిర్మాణం కల్గిఉండునని భావించాడు.
భౌతిక ధర్మాలు
[మార్చు]భౌతిక స్థితి
[మార్చు]డైబోరాన్ రంగులేని వాయువు. అప్రియమైన తియ్యటి వాసన కల్గి ఉంది. డైబోరాన్ యొక్క అణుభారం 27.67 గ్రాములు/మోల్
సాంద్రత
[మార్చు]డైబోరాన్ సాంద్రత 1.216 గ్రాములు/లీటరుకు
ద్రవీభవన ఉష్ణోగ్రత
[మార్చు]డైబోరాన్ రసాయన పదార్థం యొక్క ద్రవీభవన స్థానం −164.85 °C (−264.73 °F;108.30K)
బాష్పీభవన ఉష్ణోగ్రత
[మార్చు]డైబోరాన్ రసాయన పదార్థం యొక్క బాష్పీభవన స్థానం −92.5 °C (−134.5 °F; 180.7K)
ద్రావణీయత
[మార్చు]నీటితో రసాయనచర్య జరుపును.
అణునిర్మాణం-బంధం
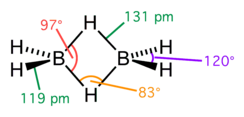
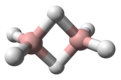
[మార్చు]డైబోరాన్ అణువు నాలుగు చివరి/అంచులను, వాటిని కలుపుతూ (bridging) రెండుహైడ్రోజన్ పరమాణువులతో D2h సౌష్టవనిర్మాణం కల్గిఉన్నది. ఈ అణునిర్మాణ మాదిరిని మాలిక్యులర్ఆర్బిటాల్ థియరీ ప్రకారం నిర్ణయించారు. అణువులో బోరాన్, టర్మినల్ హైడ్రోజన్ పరమాణువుల మధ్య బంధాలు సంప్రాదాయ ( conventiona)2-center, 2- ఎలక్ట్రాన్ కోవాలెంట్ బంధాలు (electron covalent bonds). అణువులో బోరాన్, హైడ్రోజ పరమాణువుల మధ్య బంధం, హైడ్రోకార్బన్లలో ఉన్న బంధాలకన్న భిన్నమైనది.
B-H bridge/వంతెన కట్టు బంధాల దూరం 1.33 Å, B-H terminal/అంతిమ బంధాల దూరం1.19 Å.ఈ రెండురకాల బంధాల దూరం/పొడవులలోని వ్యత్యాసం, ఆబంధాల దృఢత్వం పై ప్రభావాన్ని కనపర్చును.B-H bridge బంధాలు కొంత వరకు బలహినమైనవి.ఈ బంధ బలహీనత, అణువును ఇన్ఫ్రరెడ్ స్పెక్ట్రం (infrared spectrum) లోఉండగా ఏర్పడిన వైబ్రేసనల్ సిగ్నేచరులను బట్టి వాటి బలహీనతను గుర్తించవచ్చును.అందులో B-H bridge, B-H terminal బంధాల వైబ్రేసనల్ సిగ్నేచరువరుసగా ~2100, 2500 సెం.మీ−1.
ఉత్పత్తి
[మార్చు]డైబోరాన్ మీద జరిపిన విశ్రుత అధ్యయనంతో పలుపద్ధతులలో డైబోరాన్ను సంశ్లేషణ చేయుటకు మార్గం సులభతరం అయ్యింది.ఎక్కువ ఉత్పత్తి రసాయనచర్యలలో హైడ్రైడ్ దాతలు (hydride donors) బోరాన్ హైలైడులు/హలినాయిడ్స్ లేదా అల్కఆక్సైడ్లతో రసాయన చర్య జరిపించి డైబోరాన్ ను ఉత్పత్తి కావించెదరు.
పారిశ్రామిక ఉత్పత్తిలో బోరాన్ ట్రైఫ్లోరైడ్ ను సోడియం హైడ్రైడ్, లిథియం హైడ్రైడ్ లేదా లిథియం అల్యూమినియం హైడ్రైడ్తో క్షయికరించడం ద్వారా ఉత్పత్తి చేయుదురు.
- 8 BF3 + 6 LiH → B2H6 + 6 LiBF4
ప్రయోగశాలలో రెండురకాల విధానాలలో ఉత్పత్తి కావించెదరు.బోరాన్ ట్రైక్లోరైడ్ ను లిథియం అల్యూమినియం హైడ్రైడ్ తో చర్య జరిపించడం వలన, లేదా బోరాన్ ట్రైఫ్లోరైడ్ ఈథర్ ద్రావణాన్నిసోడియం బోరోహైడ్రైడ్ తో చర్య వలన డైబోరాన్ ను ఉత్పత్తి చేస్తారు.
- 4 BCl3 + 3 LiAlH4 → 2 B2H6 + 3 LiAlCl4
- 4 BF3 + 3 NaBH4 → 2 B2H6 + 3 NaBF4
పాతపద్ధతులలో బోరో హైడ్రైడ్ లవణాలు పాస్పారిక్ ఆమ్లం లేదా విలీన సల్ఫ్యూరిక్ ఆమ్లం వంటి నాన్-అక్సిడైసింగు ఆమ్లాలతో నేరుగా రసాయనచర్య జరగండం వలన కుడా డైబోరాన్ ఏర్పడును.
- 2 BH4− + 2 H+ → 2 H2 + B2H6
అలాగే లఘుస్థాయిలో తక్కువ ప్రమాణంలో అవసరమైనచో బోరో హైడ్రైడ్లను ఆక్సీకరించడం ద్వారా డైబోరాన్ను ఉత్పత్తి చేస్తారు. ఉదాహరణకు అయోడిన్^ను ఆక్సీకరణ కారకంగా వాడిన సమీకరణం:
- 2 NaBH4 + I2 → 2 NaI + B2H6 + H2
మరొక లఘుస్థాయి ఉత్పత్తి ప్రక్రియలో హైడ్రోబోరేట్, పాస్ఫారిక్ ఆమ్లాలను ప్రారంభిక పదార్థాలుగా వాడి ఉత్పత్తి చేయుదు��ు.
రసాయన చర్యలు
[మార్చు]డైబోరాన్ అత్యంత చర్యాశీలత ఉన్న రసాయనపదార్థం, విభిన్నమైన రసాయనకారకం, అందుచే పలు రకాలుగా వినియోగిస్తారు.లేవిస్ క్షారాలతో అడక్ట్స్ (adducts:రెండు సంయోగ పదార్థాల మధ్య అదనపు చర్య వలన ఏర్పడు పదార్థాలు) ఏర్పరచును.ఇలాంటి అడక్ట్స్/adducts చురుకుగా ఇతర ఉత్పత్తులను ఏర్పరచును.డైబోరాన్, అమ్మోనియాతో చర్యవలన డై బోరాన్ యొక్క డైఅమ్మోనియేట్ ను ఏర్పరచును.అల్కీన్స్ తో కూడా చర్య జరుపును.
నీటితో డైబోరాన్ చర్యవలన హైడ్రోజన్, బోరిక్ ఆమ్లం ఏర్పడును.
- B2H6 + 6H2O → 2B(OH)3 + 6H2
మిథనాల్ తో డైబోరాన్ చర్యజరపడం వలన హైడ్రోజన్, ట్రైమిథోక్సిబోరేట్ ఎస్టరు ఏర్పడును.
- B2H6 + 6 MeOH → 2 B(OMe)3 + 6 H2
డైబోరాన్ తో సోడియం ఆమాల్గమ్ చర్యతో NaBH4, Na[B3H8] ఉత్పన్నమగును. డైఇథైల్ ఈథర్ ద్రావణంలో లిథియం హైడ్రైడ్ తో చర్య వలన లిథియంబోరో హైడ్రైడ్ ఏర్పడును.
- B2H6 + 2 LiH → 2 LiBH4
హైడ్రోజన్ క్లోరైడ్ లేదా హైడ్రోజన్ బ్రోమైడ్ వాయువుతో డైబోరాన్ చర్య వలన బోరాన్ హలో హైడ్రైడ్ ఏర్పడును.
- B2H6 + HX → B2H5X + H2 (X = Cl, Br)
20 బార్ పీడనం వద్ద, 470K ఉష్ణోగ్రత దగ్గర కార్బన్ మొనాక్సైడ్తో చర్య వలన H3BCO ఏర్పడును.
అనువర్తనాలు
[మార్చు]రాకెట్ చోదకంగా అనుకూలమైనదిగా భావించి ప్రయోగాత్మాకంగా డైబోరాన్ ను ఉపయోగించి చూసారు. కాని డైబోరాన్ను సర్వీస్ రాకెట్లలో వాడలేదు. దీనిని రబ్బరు వోల్కనైజరులో ఉపయోగిస్తారు.హైడ్రోకార్బన్ల పాలిమెరిజెసన్ లో ఉత్ప్రేరకంగా (catalyst, జ్వాల వేగనియంత్రిణి/వేగవృద్ధినిగా (flame-speed accelerator, అర్ద వాహకాలలో (semiconductors) డోపింగ్ కారకంగా డైబోరాన్ను ఉపయోగిస్తారు. సెమి కండక్టరు/అర్దవాహకాల తయారికి అవసరమైన శుద్ధబోరాన్ ఉత్పత్తికి దీనిని మధ్యమస్థాయి రసాయనంగా వాడెదరు.
రక్షణ-ఆరోగ్యం పై ప్రభావం
[మార్చు]దీర్ఘ కాలం తక్కువ మోతాదులో/ప్రమాణంలో డైబోరాన్ ప్రభావానికి గురైన జనాలు శ్వాస సంబంధ ఇరిటేసన్ ఇబ్బందులకు, కండరాలు పట్టివెయ్యడం (seizures), ఆయాసము (fatigue) మగతగా drowsiness ఉండటం, అయోమయం (confusion), అప్పుడప్పుడు నిలకడలేని వణుకుతనం వంటి లక్షణాలకులోనవుతారు.
మూలాలు/ఆధారాలు
[మార్చు]- ↑ 1.0 1.1 1.2 1.3 1.4 1.5 NIOSH Pocket Guide to Chemical Hazards. "#0183". National Institute for Occupational Safety and Health (NIOSH).
- ↑ 2.0 2.1 "Diborane". Immediately Dangerous to Life and Health Concentrations (IDLH). National Institute for Occupational Safety and Health (NIOSH).
- ↑ "International Chemical Safety Cards - Diborane". CDC/NIOSH ICSC Database. NIOSH Education and Information Division. Archived from the original on 24 సెప్టెంబరు 2015. Retrieved 14 August 2015.