Triklornitrometan
| Klorpikrin | |
  | |
| Systematiskt namn | Triklornitrometan |
|---|---|
| Övriga namn | Klorpikrin, Nitrokloroform, PS |
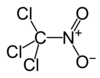
| Kemisk formel | CCl3NO2 |
| Molmassa | 164,375 g/mol |
| Utseende | Färglös vätska |
| CAS-nummer | 76-06-2 |
| SMILES | ClC(Cl)(Cl)[N+](=O)[O-] |
| Egenskaper | |
| Densitet | 1,692 g/cm³ |
| Löslighet (vatten) | 1,7 g/l |
| Smältpunkt | -69,2 °C |
| Kokpunkt | 112,4 °C |
| Faror | |
| Huvudfara | |
| NFPA 704 | |
| LD50 | 250 mg/kg |
| SI-enheter & STP används om ej annat angivits | |
Triklornitrometan eller klorpikrin är en klorerad och nitrerad organisk förening med kemisk formel CCl3NO2. Triklornitrometan är mycket giftigt och explosivt.
Historia
Triklornitrometan framställdes första gången 1848 av den skotske kemisten John Stenhouse genom att blanda natriumhypoklorit (NaClO) med pikrinsyra (C6H2OH(NO2)3).
Eftersom han använde pikrinsyra som reaktant kallade han ämnet för klorpikrin trots att de inte har någon strukturell likhet.
Framställning
Triklornitrometan framställs industriellt genom att blanda nitrometan (CH3NO2) och natriumhypoklorit (NaClO).
Användning
Under första världskriget användes klorpikrin som kemiskt stridsmedel. Även om den inte är lika skadlig eller dödlig som andra stridsgaser fungerar den som tårgas och framkallar kräkningar. När soldater som utsatts för klorpikrin tar av sig skyddsmasken för att kräkas utsätts de för andra, dödligare stridsgaser.
Idag används klorpikrin i liten skala som bekämpningsmedel mot djur som gömmer sig under mark som råttor, kaniner etc. Det används i kombination med andra bekämpningsmedel som t.ex. metylbromid.
Källor
Se även
- Den här artikeln är helt eller delvis baserad på material från engelskspråkiga Wikipedia, Chloropicrin.




