Бакар(I)-хлорид
Изглед

| |
| |
| Називи | |
|---|---|
| IUPAC назив
Бакар(I)-хлорид
| |
| Идентификација | |
| ECHA InfoCard | 100.028.948 |
| MeSH | Copper+chloride |
| RTECS | GL6990000 |
| Својства | |
| CuCl | |
| Моларна маса | 98,99 g/mol |
| Агрегатно стање | бели прах, сув зелен због оксидације од нечистоћа |
| Густина | 4,140 g/cm3, основно |
| Тачка топљења | 430°C (703 K) |
| Тачка кључања | 1490°C (1760 K), разлаже се |
| 0.0062 g/100 mL (20 °C) | |
| Структура | |
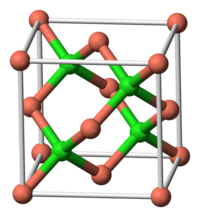
| Кристална решетка/структура | Тетраедар „густо паковање“ (структура цинк-сулфида) |
| Опасности | |
| Главне опасности | Иритант |
| R и S-ознаке | R: R22, R50, R53 S: S22, S60, S61 |
| NFPA 704 | |
| Сродна једињења | |
Други анјони
|
Бакар(I)-бромид Бакар(I)-јодид |
Други катјони
|
Бакар(II)-хлорид Сребро(I)-хлорид |
Уколико није другачије напоменуто, подаци се односе на стандардно стање материјала (на 25°C [77°F], 100 kPa). | |
| Референце инфокутије | |
Бакар(I)-хлорид (купро-хлорид) је неорганско хемијско једињење хемијске формуле CuCl.
Добијање
[уреди | уреди извор]- Загревањем раствора куприхлорида у концентрованој хлороводоничној киселини са металним бакром, обично у облику опиљака:
- CuCl2 + Cu → 2CuCl
- Провођењем сумпор-диоксида кроз раствор куприсулфата и натријум-хлорида:
- 2CuSO4 + 2NaCl + SO2 + 2H2O → 2CuCl + 2NaHSO4 + H2SO4
У оба случаја, добијени талог се одвоји цеђењем, испира се и суши.[1]
Физичко-хемијске особине
[уреди | уреди извор]Купро-хлорид је бела чврста супстанца, нерастворна у води. На ваздуху постепено добија зелену боју услед грађења базног куприхлорида (CuCl2•3CuO•3H2O). Са хлороводоничном киселином гради комплексна једињења. Са амонијаком такође гради комплексно једињење, чији безбојан раствор на ваздуху постаје затвореноплав. Пошто лако апсорбује угљен-моноксид, у ту сврху се и употребљава. Овај (амонијачни) раствор апсорбује и ацетилен при чему се гради црвени талог купро-ацетилида, иначе експлозивно једињење, а које представља доказ за присуство ацетилена.[1]
Извори
[уреди | уреди извор]- ^ а б Parkes, G.D. & Phil, D. 1973. Мелорова модерна неорганска хемија. Научна књига. Београд.

