Thymocyt


Een thymocyt is een immuuncel die in de thymus aanwezig is, voordat deze in een T-cel verandert.[1] Thymocyten worden als stamcellen in het beenmerg geproduceerd en bereiken de thymus via het bloed. Ze komen in de cortex voor en in mindere mate in de medulla van de thymus, die daardoor een donkerdere kleur heeft dan de medulla. Witte bloedcellen en T-cellen zijn immuuncellen.
In de eerste fase worden prothymocyten of vroege thymocyten gevormd, die hun genen die coderen voor T-celantigeenreceptoren nog niet hebben herschikt of daar net mee beginnen.
In de tweede fase verschijnt de T-celreceptor TCR, die uit alfa- en bèta- of gamma- en deltaketens bestaat, maar meestal uit alfa- en bètaketens. De genetische loci die de alfa-keten en bèta-keten van T-celreceptoren coderen, bevinden zich op verschillende chromosomen. Net als bij B-celreceptoren bevatten de TCR loci aparte V, D en J-segmenten die tijdens de ontwikkeling van T-cellen in de thymus recombineren en op een unieke wijze bij elkaar worden gebracht.
Ten slotte gaat in het laatste stadium van de celdifferentiatie, bij de volwassen thymocyt CD1 verloren en worden er twee grote subpopulaties gegenereerd die in het bloed terechtkomen: een die CD4[2] bewaart en CD8 verliest en een andere die CD4 verliest en CD8 bewaart.[3] CD4 zijn T-helpercellen en CD8 zijn cytotoxische T-cellen.
Thymopoiese is het proces dat volgens negatieve of positieve selectie thymocyten in volwassen T-cellen verandert. Deze selectie is van vitaal belang bij het vormen van de populatie thymocyten tot voldoende T-cellen die in staat zijn om op vreemde pathogenen te reageren, maar de thymocyten moeten ook voor de eigen antigenen van het lichaam tolerant blijven.
Positieve selectie selecteert cellen die in staat zijn om MHC-moleculen van klasse I of II met ten minste een zwakke affiniteit te binden. Dit elimineert, door een proces dat 'dood door verwaarlozing' wordt genoemd, die T-cellen die niet-functioneel zijn omdat zij geen MHC kunnen binden. Negatieve selectie vernietigt thymocyten met een hoge affiniteit voor eigen peptiden of MHC. Dit elimineert cellen die voor immuunreacties zorgen in de eigen eiwitten. Negatieve selectie is niet 100% effectief en sommige autoreactieve T-cellen ontsnappen en komen in de bloedsomloop terecht. Er bestaan aanvullende mechanismen van perifere tolerantie om deze cellen onschadelijk te maken, zoals deletie, de regulatoire T-cel en anergie, dat is de afwezigheid van een reactie van de verdedigingsmechanismen van het lichaam op vreemde stoffen. Als deze ook falen kan er auto-immuniteit ontstaan.
98% van de zich ontwikkelende T-cellen sterven in de cortex en worden gefagocyteerd door aanwezige macrofagen.
Stadia van rijping
[bewerken | brontekst bewerken]Thymocyten worden in een aantal verschillende rijpingsstadia ingedeeld op basis van de expressie van celoppervlaktemarkers. Het vroegste thymocytstadium is het dubbel negatieve stadium, negatief voor zowel CD4 als CD8, dat recent beter is beschreven is als typering-negatief en dat in vier substadia kan worden onderverdeeld. Het volgende belangrijke stadium is het dubbel positieve stadium, positief voor zowel CD4 als CD8, en het laatste stadium tijdens de rijping is het enkelvoudige positieve stadium, positief voor CD4 of CD8.
Bij muizen
[bewerken | brontekst bewerken]| stadium | oppervlaktemerkers voor typering | locatie | gebeurtenissen |
|---|---|---|---|
| dubbel negatief 1 DN1 of ETP, vroege T-lijn Progenitor |
typering-CD44+CD25-CD117+ | cortex | proliferatie, verlies van B-cel en beenmerg potenties |
| dubbel negatief 2 DN2 | typering-CD44+CD25+CD117+ | cortex | - |
| dubbel negatief 3 DN3 | typering-CD44-CD25+ | cortex | TCR-bèta-herschikking, bèta-selectie |
| dubbel negatief 4 DN4 | typering-CD44-CD25- | cortex | - |
| dubbel positief | CD4+CD8+ | cortex | TCR-alfa herschikking, positieve selectie, negatieve selectie |
| enkelvoudig positief | CD4+CD8- of CD4-CD8+ | medulla | negatieve selectie |
Bij de oppervlaktemerkers voor typering wordt de CD-nomenclatuur aangehouden.
Bij mensen
[bewerken | brontekst bewerken]Bij mensen bevinden circulerende CD34+ hematopoëtische stamcellen zich in het beenmerg. Ze produceren voorlopers van T-cellen, die naar de thymus gaan en zo thymocyten worden, en differentiëren onder invloed van het Notch-eiwit en zijn liganden.
Vroege, dubbel negatieve thymocyten brengen CD2, CD5 en CD7 tot expressie en kunnen daardoor worden geïdentificeerd. Nog tijdens het dubbel negatieve stadium stopt de CD34-expressie en wordt CD1 tot expressie gebracht. Expressie van zowel CD4 als CD8 maakt ze dubbel positief en rijpt uit tot CD4+- of CD8+-cellen.[4]
Gebeurtenissen tijdens rijping
[bewerken | brontekst bewerken]Kolonisatie van de thymus
[bewerken | brontekst bewerken]
humoral – humorale afweer
cellular – cellulaire afweer
Thymocyten komen uit de hematopoëtische voorlopercellen voort uit het beenmerg. Zij bereiken de thymus via de bloedsomloop.[5] Het aantal voorlopercellen dat elke dag de thymus binnenkomt, wordt als klein beschouwd. Daarom is het onbekend welke voorlopercellen de thymus koloniseren. Momenteel wordt voorgesteld dat vroege lymfoïde voorlopercellen (ELP) de thymus koloniseren en waarschijnlijk de voorlopers zijn van ten minste enkele thymocyten. ELP's zijn celtyperinge CD44+CD25-CD117+ en lijken dus sterk op ETP's, de vroegste voorlopercellen in de thymus. Voorlopercellen komen de thymus binnen via de cortico-medullaire verbinding. Moleculen waarvan bekend is dat ze belangrijk zijn voor de binnenkomst van de thymus, zijn onder meer P-selectine (CD62P) en de chemokine-receptoren CCR7 en CCR9.[6]
Na de binnenkomst in de thymus prolifereren voorlopers om de ETP-populatie (ETP: vroege T-lijn Progenitor) te vormen. Deze stap wordt gevolgd door de vorming van DN2-thymocyten (DN: dubbel negatief) die migreren van de cortico-medullaire verbinding naar het thymuskapsel. De thymus bestaat uit twee lobben die bedekt zijn met een vezelig kapsel. DN3-thymocyten worden gegenereerd in de subkapselaire zone.
Naast proliferatie vinden differentiatie en T-celtypering-commitment plaats binnen de DN-thymocytenpopulatie. Commitment, of verlies van alternatieve typering-potenties (zoals beenmerg, B- en NK-typering-potenties), is afhankelijk van Notch-signalering en is voltooid in het DN3-stadium. Na T-celtypering-commitment ondergaan DN3-thymocyten bèta-selectie.[7]
Bèta-selectie
[bewerken | brontekst bewerken]

Het vermogen van T-cellen om vreemde antigenen te herkennen wordt gemedieerd door de T-celreceptor, een oppervlakte-eiwit dat korte eiwitsequenties (peptiden) kan herkennen die op MHC worden gepresenteerd. Het doel van de ontwikkeling van thymocyten is om volwassen T-cellen te produceren met een diverse reeks functionele T-celreceptoren, door middel van het proces van T-celreceptoren-genherschikking.
In tegenstelling tot de meeste genen, die een stabiele sequentie hebben in elke cel die ze tot expressie brengt, bestaat de T-celreceptor uit een reeks alternatieve genfragmenten. Om een functionele T-celreceptor te creëren, gebruiken de dubbel negatieve thymocyten een reeks DNA-interagerende enzymen om het DNA te knippen en afzonderlijke genfragmenten bij elkaar te brengen. De uitkomst van dit proces is dat elke T-celreceptor een andere nucleotidesequentie heeft, als gevolg van een andere keuze van genfragmenten en de fouten die worden geïntroduceerd tijdens het knip- en verbindingsproces (zie het gedeelte over V(D)J-recombinatie voor meer informatie over T-celreceptoren-herschikking). Het evolutionaire voordeel van het hebben van een groot aantal unieke T-celreceptoren is dat elke T-cel in staat is een ander peptide te herkennen, wat een verdediging biedt tegen zich snel aanpassende pathogenen.[8]
T-celreceptor-herschikking vindt plaats in twee stappen. Eerst wordt de T-celreceptor-bèta-keten herschikt in het DN3-stadium van de ontwikkeling van T-cellen. De T-celreceptor-bèta-keten wordt gepaard met de pre-T-cel-alfa om de pre-T-celreceptor te genereren. Het cellulaire nadeel in het herschikkingsproces is dat veel van de combinaties van de T-celreceptorgenfragmenten niet-functioneel zijn. Om thymocyten te elimineren die een niet-functionele T-celreceptor hebben gemaakt, mogen alleen cellen die de bètaketen succesvol hebben herschikt om een functionele pre-T-celreceptor te produceren, zich ontwikkelen voorbij het DN3-stadium. Cellen die er niet in slagen een functionele pre-T-celreceptor te produceren, worden geëlimineerd door apoptose. Dit proces wordt het bètaselectiecontrolepunt genoemd. Succesvolle bètaselectie vereist dat T-celreceptor-bèta wordt geproduceerd, T-celreceptor-bèta in staat is om te paren met pre-T-cel-alfa om de pre-T-celreceptor te genereren, en dat de pre-T-celreceptor op het celoppervlak kan interacteren met de T-celreceptor-signaaleiwitten.
In de bèta-selectiefase vormt de pre-T-celreceptor, net als de volwassen T-celreceptor, ook een immunologische synaps.[9] Een immunologische synaps is de interface tussen een antigeenpresenterende cel of doelwitcel en een T-cel. Hoewel de interactie tussen pre-T-celreceptor en peptide-gebonden MHC niet essentieel is voor de ontwikkeling van T-cellen,[10][11] speelt het een cruciale rol bij het aanmoedigen van de preferentiële proliferatie van cellen waarvan de pre-T-celreceptor eigen-MHC kan binden.[12][13]
Na bèta-selectie genereren thymocyten CD4+CD8+ dubbel positieve cellen, die vervolgens een T-celreceptor-alfa-herschikking ondergaan, wat resulteert in een volledig samengestelde T-celreceptor.
Positieve selectie en celtypering commitment
[bewerken | brontekst bewerken]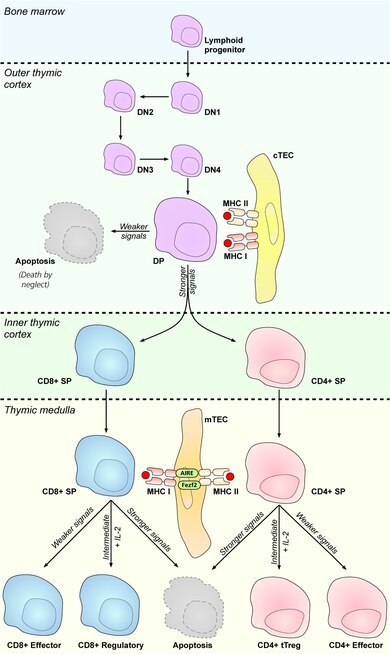
DP – dubbel positef
SP – enkelvoudig positief
cTEC – corticale thymische epitheelcellen
mTEC – medullaire thymische epitheelcellen
Treg – regulatoire T-cel
Thymocyten die bèta-selectie doorstaan, brengen een T-celreceptor tot expressie die zich op het celoppervlak kan verzamelen. Veel van deze T-celreceptoren zullen echter nog steeds niet-functioneel zijn, vanwege een onvermogen om MHC te binden. De volgende belangrijke fase van de ontwikkeling van thymocyten is positieve selectie, om alleen die thymocyten te behouden die een T-celreceptor hebben die MHC kan binden. De T-celreceptor heeft CD8 nodig als coreceptor om te binden aan MHC klasse I, en CD4 als coreceptor om te binden aan MHC klasse II. In deze fase upreguleren thymocyten zowel CD4 als CD8, en worden ze dubbel positieve cellen.
Dubbel positieve thymocyten die een T-celreceptor hebben die MHC klasse I of klasse II kan binden (zelfs met een zwakke affiniteit) ontvangen signalering via de T-celreceptor. Thymocyten met een T-celreceptor die niet in staat is om MHC-klasse I of klasse II te binden, ondergaan apoptose. Sommige thymocyten zijn in staat om mislukte positieve selectie te redden door receptorbewerking (herschikking van het andere T-celreceptorallel om een nieuwe T-celreceptor te produceren).
De dubbel positieve thymocyten ondergaan celtypering commitment, en rijpen tot een CD8+ T-cel (die MHC-klasse I herkent) of een CD4+ T-cel (die MHC-klasse II herkent). Celtypring commitment vindt plaats in het late stadium van positieve selectie en werkt door downregulatie van zowel CD4 als CD8 (het verminderen van het signaal van de T-celreceptor) en vervolgens upregulatie van alleen CD4. Thymocyten die weer signalen beginnen te ontvangen, zijn die welke MHC-klasse II herkennen en ze worden CD4+ T-cellen. Thymocyten die geen signalen meer beginnen te ontvangen, zijn die welke MHC-klasse I herkennen en ze downreguleren CD4 en upreguleren CD8, om CD8+ T-cellen te worden. Beide typen thymocyten staan bekend als enkelvoudig positieve thymocyten.
Negatieve selectie
[bewerken | brontekst bewerken]Succes bij positieve selectie zorgt ervoor dat de thymocyt een aantal rijpingsveranderingen ondergaat tijdens de overgang naar een enkelpositieve T-cel. De enkelpositieve T-cellen reguleren de chemokine-receptor CCR7 omhoog, wat leidt tot migratie van de cortex naar de medulla. In dit stadium omvat het belangrijkste rijpingsproces negatieve selectie, de eliminatie van autoreactieve thymocyten.
Het belangrijkste nadeel van een genherschikkingsproces voor T-celreceptoren is dat door toeval enkele rangschikkingen van genfragmenten een T-celreceptor zullen ontstaan die in staat zijn om eigen peptiden te binden die worden gepresenteerd op MHC-klasse I of MHC-klasse II. Als T-cellen met deze T-celreceptoren de periferie zouden binnendringen, zouden ze in staat zijn om een immuunreactie tegen zichzelf te activeren, wat resulteert in auto-immuniteit. Negatieve selectie is het proces dat is ontwikkeld om dit risico te verminderen. Tijdens negatieve selectie worden alle thymocyten met een hoge affiniteit voor binding van eigen peptiden gepresenteerd op MHC klasse I of klasse II geïnduceerd om BCL2L11 te upreguleren, een proteïne dat apoptose aanstuurt. Cellen die geen hoge affiniteit hebben voor eigen antigenen overleven negatieve selectie. In dit stadium worden sommige cellen ook geselecteerd om regulatoire T-cellen te worden, meestal cellen die een intermediaire affiniteit hebben voor hun eigen peptide.
Negatieve selectie kan optreden in de dubbel positieve fase in de cortex. Het repertoire van peptiden in de cortex is echter beperkt tot die welke tot expressie worden gebracht door epitheelcellen, en dubbel positieve cellen zijn slecht in het ondergaan van negatieve selectie. Daarom is de belangrijkste plaats voor negatieve selectie de medulla, zodra cellen zich in de enkelpositieve fase bevinden. Om thymocyten te verwijderen die reactief zijn op perifere organen, sturen de transcriptiefactoren Aire (Autoimmune regulator) en Fezf2 (FEZ family zinc finger 2) de expressie van meerdere perifere antigenen aan, zoals insuline, wat resulteert in deletie van cellen die specifiek zijn voor die antigenen.[14][15] Hierdoor kunnen enkelvoudigpositieve thymocyten worden blootgesteld aan een complexere set van eigen-antigenen dan aanwezig is in de cortex, en worden daarom efficiënter die T-cellen verwijderd die autoreactief zijn.
Enkelvoudige positieve thymocyten blijven 1-2 weken in de medulla, waarbij ze eigen-antigenen onderzoeken om te testen op autoreactiviteit. Gedurende deze tijd ondergaan ze laatste rijpingsveranderingen en verlaten ze vervolgens de thymus met behulp van S1P en CCR7. Bij binnenkomst in de perifere bloedbaan worden de cellen beschouwd als volwassen T-cellen en niet als thymocyten.
Negatieve selectie is niet 100% effectief, sommige autoreactieve T-cellen ontsnappen aan thymuscensuur en worden in de bloedsomloop vrijgegeven. Er bestaan aanvullende mechanismen van perifere tolerantie die actief zijn in de periferie om deze cellen tot zwijgen te brengen, zoals deletie, regulatoire T-cellen en anergie. Anergie is de afwezigheid van een reactie van de verdedigingsmechanismen van het lichaam op vreemde stoffen. Als deze perifere tolerantiemechanismen ook falen, kan er auto-immuniteit ontstaan.
Thymustransplantatie resulteert erin dat T-cellen worden geleerd om in plaats daarvan niet te reageren met donorantigenen en kunnen nog steeds reageren met veel eign-antigenen in het lichaam. Auto-immuunziekte is een veelvoorkomende complicatie na thymustransplantatie, die bij 42% van de proefpersonen wordt aangetroffen na 1 jaar na de transplantatie.[16] Dit wordt echter gedeeltelijk verklaard door het feit dat de indicatie zelf, namelijk het volledige velocardiofaciaal syndroom (afwezigheid van thymus), het risico op auto-immuunziekte vergroot.[17]
Samenvatting
[bewerken | brontekst bewerken]| type | functioneel bèta-selectie |
functioneel positieve selectie |
autoreactief negatieve selectie |
| locatie | cortex | cortex | cortex/medulla |
 DN: dubbel negatief DP: dubbel postief SP: enkelvoudig positief |
De structurele eigenschappen van de bèta-keten van de T-celreceptor die door de thymocyt is herschikt moet om het bèta-selectiecontrolepunt te passeren behouden blijven, waardoor deze met pre-TCRα op het oppervlak van de thymocyte kan worden gepresenteerd. Dit elimineert thymocyten met grove defecten die door genherschikking in de T-celreceptor zijn geïntroduceerd. |
Om positief geselecteerd te worden, moeten thymocyten interacteren met verschillende celoppervlakmoleculen, MHC, om reactiviteit en specificiteit te garanderen.[18] |
Negatieve selectie is de actieve inductie van apoptose in thymocyten met een hoge affiniteit voor eigen peptiden of MHC. |
- voetnoten
- ↑ "thymocyte" at Dorland's Medical Dictionary
- ↑ CD is de afkorting van Cluster of differentiation.
- ↑ Inmunolog - G2051223: Inmunoloxía Médica - StuDocu». StuDocu. Geraadplegd op 26 september 2018.
- ↑ afbeelding 12-13 in: Robbins Basic Pathology. Saunders, Philadelphia (2007). ISBN 978-1-4160-2973-1. 8th edition.
- ↑ Schwarz BA, Bhandoola A. Trafficking from the bone marrow to the thymus: a prerequisite for thymopoiesis. Immunol Rev 209:47, 2006. volledige tekst
- ↑ BA Schwarz, A Sambandam, I Maillard, BC Harman, PE Love PE en A Bhandoola. Selective thymus settling regulated by cytokine and chemokine receptors, 15 februari 2007. voor The Journal of Immunolgy 178, 4, 2008-17
- ↑ C. Clare Blackburn & Nancy R. Manley "Developing a new paradigm for thymus organogenesis" Nature Reviews Immunology April 2004 278-289 Retrieved 10/4/12 [1]
- ↑ Sleckman BP, Lymphocyte antigen receptor gene assembly: multiple layers of regulation. Immunol Res 32:153-8, 2005. volledige tekst.
- ↑ (en) Allam, Amr H., Charnley, Mirren, Pham, Kim, Russell, Sarah M. (1 maart 2021). Developing T cells form an immunological synapse for passage through the β-selection checkpoint. Journal of Cell Biology 220 (3): e201908108. ISSN: 0021-9525. PMID 33464309. PMC 7814350. DOI: 10.1083/jcb.201908108.
- ↑ (en) Irving, Bryan A., Alt, Frederick W., Killeen, Nigel (8 mei 1998). Thymocyte Development in the Absence of Pre-T Cell Receptor Extracellular Immunoglobulin Domains. Science 280 (5365): 905–908. ISSN: 0036-8075. PMID 9572735. DOI: 10.1126/science.280.5365.905.
- ↑ Koller, Beverly H., Marrack, Philippa, Kappler, John W., Smithies, Oliver (1 mei 2010). Normal development of mice deficient in beta 2M, MHC class I proteins, and CD8+ T cells. 1990. Journal of Immunology 184 (9): 4592–4595. ISSN: 1550-6606. PMID 20410496.
- ↑ Mizsei, Réka, Li, Xiaolong, Chen, Wan-Na, Szabo, Monika, Wang, Jia-huai (January 2021). A general chemical crosslinking strategy for structural analyses of weakly interacting proteins applied to preTCR-pMHC complexes. Journal of Biological Chemistry 296: 100255. ISSN: 0021-9258. PMID 33837736. PMC 7948749. DOI: 10.1016/j.jbc.2021.100255.
- ↑ (en) Li, Xiaolong, Mizsei, Réka, Tan, Kemin, Mallis, Robert J., Duke-Cohan, Jonathan S. (8 januari 2021). Pre–T cell receptors topologically sample self-ligands during thymocyte β-selection. Science 371 (6525): 181–185. ISSN: 0036-8075. PMID 33335016. PMC 8011828. DOI: 10.1126/science.abe0918.
- ↑ Anderson, M.S. et al. (2002) Projection of an Immunological Self-Shadow Within the Thymus by the Aire Protein. Science 298 (5597), 1395-1401
- ↑ Takaba, H. et al. (2015) Fezf2 Orchestrates a Thymic Programs of Self-Antigen Expression for Immune Tolerance. Cell 163, 975 - 987
- ↑ Thymus Transplantation Book Thymus Gland Pathology, pages 255-267, Springer Milan 2008 DOI:10.1007/978-88-470-0828-1 ISBN 978-88-470-0827-4 (Print) ISBN 978-88-470-0828-1 (Online) DOI:10.1007/978-88-470-0828-1_30
- ↑ Markert ML, Devlin BH, Alexieff MJ, etal (May 2007). Review of 54 patients with complete DiGeorge anomaly enrolled in protocols for thymus transplantation: outcome of 44 consecutive transplants. Blood 109 (10): 4539–47. PMID 17284531. PMC 1885498. DOI: 10.1182/blood-2006-10-048652.
- ↑ (2004). De vierde manier? Het benutten van agressieve tendensen in de thymus. J Immunol 173 (11): 6515–20. PMID 15557139. DOI: 10.4049/jimmunol.173.11.6515.
- bronvermelding
- Dit artikel of een eerdere versie ervan is een (gedeeltelijke) vertaling van het artikel Thymocyte op de Engelstalige Wikipedia, dat onder de licentie Creative Commons Naamsvermelding/Gelijk delen valt. Zie de bewerkingsgeschiedenis aldaar.
