Goud(I)chloride
Uiterlijk
| Goud(I)chloride | ||||
|---|---|---|---|---|
| Structuurformule en molecuulmodel | ||||
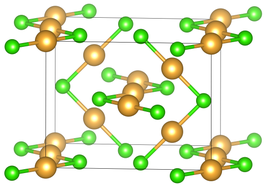
| ||||
Kristalstructuur van goud(I)chloride
| ||||
| Algemeen | ||||
| Molecuulformule | AuCl | |||
| IUPAC-naam | goud(I)chloride | |||
| Andere namen | goudchloride, goudmonochloride | |||
| Molmassa | 232,41955 g/mol | |||
| SMILES | [Au]Cl
| |||
| InChI | 1S/Au.ClH/h;1H/q+1;/p-1
| |||
| CAS-nummer | 10294-29-8 | |||
| EG-nummer | 233-655-8 | |||
| PubChem | 27366 | |||
| Wikidata | Q2371753 | |||
| Waarschuwingen en veiligheidsmaatregelen | ||||
| ||||
| H-zinnen | H314 - H317 | |||
| EUH-zinnen | geen | |||
| P-zinnen | P280 - P305+P351+P338 - P310 | |||
| Fysische eigenschappen | ||||
| Aggregatietoestand | vast | |||
| Kleur | geel | |||
| Dichtheid | 7,6 g/cm³ | |||
| Smeltpunt | 298 °C | |||
| Goed oplosbaar in | organische oplosmiddelen | |||
| Slecht oplosbaar in | water | |||
| Geometrie en kristalstructuur | ||||
| Kristalstructuur | tetragonaal | |||
| Tenzij anders vermeld zijn standaardomstandigheden gebruikt (298,15 K of 25 °C, 1 bar). | ||||
| ||||
Goud(I)chloride is een anorganische verbinding van goud en chloor met als brutoformule AuCl, waarin goud zich in oxidatietoestand +1 bevindt. Het behoort tot de goudhalogeniden. Goud(I)chloride ontstaat bij thermische ontleding van goud(III)chloride boven een temperatuur van 298°C. Het is een gele vaste stof die zeer slecht oplosbaar is in water.
Reacties
[bewerken | brontekst bewerken]De verbinding is weinig stabiel. Bij verhitting met water disproportioneert goud(I)chloride in metallisch goud en goud(III)chloride:
De reactie met kaliumbromide geeft kaliumtetrabromoauraat(III), kaliumchloride en metallisch goud:
Toxicologie en veiligheid
[bewerken | brontekst bewerken]Goud(I)chloride irriteert huid en ogen, schaadt de nieren en vermindert het aantal witte bloedcellen.




