Potassium 40
| Nom | Potassium 40 |
|---|---|
| Symbole |
40 19K 21 |
| Neutrons | 21 |
| Protons | 19 |
| Présence naturelle | 0,0117(1) %[1] |
|---|---|
| Demi-vie | 1,248(3) × 109 ans[1] |
| Produit de désintégration | 40Ca, 40Ar |
| Masse atomique | 39,96399817(6) u |
| Spin | 4−[1] |
| Excès d'énergie | −33 535,50 ± 0,06 keV[1] |
| Énergie de liaison par nucléon | 8 538,091 ± 0,001 keV[1] |
| Désintégration | Produit | Énergie (MeV) |
|---|---|---|
| β− à 89,28(11) % | 40 20Ca |
1,31109 |
| ε, β+ à 10,72(11) % | 40 18Ar |
1,5049 |
Le potassium 40, noté 40K, est l'isotope du potassium dont le nombre de masse est égal à 40 : son noyau atomique compte 19 protons et 21 neutrons avec un spin 4− pour une masse atomique de 39,963 998 2 g/mol. Il est caractérisé par un excès de masse de −33 535,5 keV et une énergie de liaison nucléaire par nucléon de 8 538,09 keV[1]. C'est un radioisotope du milieu naturel.
Radioactivité
[modifier | modifier le code]Le potassium 40 a une période radioactive de 1,248 milliard d'années. Ainsi, un gramme de 40K présente une activité de 265,2 kBq.
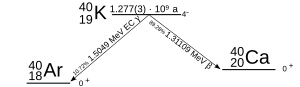
Le potassium subit concurremment trois modes de désintégration :
- une désintégration β− dans 89,28 % des cas pour donner du calcium 40, avec une énergie de désintégration de 1,311 MeV :
- une capture électronique dans 10,72 % des cas pour donner de l'argon 40, avec une énergie de désintégration de 1,505 MeV :
- une désintégration β+, en proportion négligeable en comparaison des deux réactions précédentes (de l'ordre de 0,001 %) :
La seconde réaction (capture électronique) est utilisée pour dater la formation de certaines roches contenant du potassium (méthode de « datation par le potassium-argon »), en supposant nulle la quantité initiale d'argon 40 dans ces roches et que l'argon 40 y reste piégé une fois formé. On notera que le noyau de 40
18Ar, nouvellement formé après la capture, se trouve dans un état excité (la capture vers le niveau fondamental est possible, mais rarissime). Il émet un photon lors de la désexcitation.
Il est remarquable que le potassium 40 puisse se désintégrer aussi bien en argon 40 qu'en calcium 40, car cela souligne à quel point les noyaux atomiques sont plus stables avec des nombres pairs de protons et de neutrons qu'avec des nombres impairs. De surcroît, la prépondérance de la désintégration en calcium 40 souligne l'effet stabilisateur des nombres magiques, car, avec 20 neutrons pour 20 protons, le calcium 40 est légèrement déficitaire en neutrons (par rapport aux noyaux stables voisins), mais est stabilisé par le fait qu'il est doublement magique.
Dans la mesure où le potassium est un élément indispensable à la vie, 40K constitue la principale source de radioactivité des organismes sains, supérieure à celle constituée par le carbone 14 : un homme de 70 kg subirait chaque seconde la désintégration de 4 400 atomes de 40K[2], soit environ 0,39 mSv/an par 40K contre 0,01 mSv/an imputable à 14C.
Contribution à la radioactivité naturelle
[modifier | modifier le code]Dans le corps humain
[modifier | modifier le code]Connaissant (a) la quantité totale de potassium dans un corps humain, (b) l'abondance naturelle de 40K présent dans la biosphère et (c) la période radioactive de celui-ci, il est facile de calculer le nombre de désintégrations par seconde (becquerels) qui y ont lieu.
(a) : Quantité totale de potassium dans un corps humain. Celle-ci est en moyenne de 4 216 ± 473 mmol (165 ± 18 g) pour un homme et de 4 172 ± 540 mmol (163 ± 21 g) pour une femme, mais vu que d'autres paramètres tels que l'âge ou l'IMC peuvent affecter ces valeurs, une formule qui tient compte de ces facteurs a été développée[3] comme suit :
- pour un homme : KCT = (98,3 – 0,1594 × âge + 0,1431 × poids – 0,1848 × taille) × MNG ;
- pour une femme : KCT = (94,39 – 0,1735 × âge + 0,1169 × poids – 0,1567 × taille) × MNG.
où KCT est le potassium corporel total (en mmol), l'âge est en années, le poids en kg, la taille en cm et MNG est la masse non-grasse (par exemple, pour un corps de 80 kg constitué à 20 % de graisse, la MNG vaut 0,8 × 80 = 64 kg).
(b) : L'abondance naturelle du 40K est de 0,01167 % (cf. table des isotopes du potassium).
(c) : La période radioactive du 40K (1,248 × 109 ans) permet de calculer pour une quantité donnée de l'isotope (une mmol, soit 6,022 × 1020 atomes), le nombre de désintégrations par unité de temps (en Bq). En l'occurrence, une mmol de 40K produira :
Finalement, il suffit de calculer KCT × 0,0001167 × 1,060 × 104 pour obtenir le nombre de Bq produits par le 40K dans un corps humain, ce qui en moyenne (valeurs minimales et maximales des KCT indiqués plus haut) donne donc entre 4 390 et 5 670 désintégrations par seconde (Bq). Ces valeurs sont à comparer à celles données en exemple dans la page Becquerel, où les valeurs indiquées pour l'être humain tiennent compte de façon similaire des autres isotopes naturellement présents dans le corps.
À noter qu'il est inutile de vouloir mesurer cette radioactivité à l'aide d'un compteur Geiger : les rayonnements bêta moins du 40K ne traversent que très peu la matière telle que celle qui constitue les liquides corporels ou la peau, et sont donc absorbés par les atomes des molécules environnantes, qui peuvent alors subir des ionisations. Cette mesure doit donc se faire par d'autres méthodes telles que l'homogénéisation de l'échantillon biologique suivie de la détection de son activité bêta moins par comptage de scintillation. Dans les cellules, l'ionisation de certains atomes due à la radioactivité du 40K peut provoquer la rupture de liaisons chimiques et aboutir à la formation de radicaux, qui sont généralement détoxifiés par une variété d'enzymes spécialisées. Si l'ionisation intervient sur des atomes qui constituent l'ADN des chromosomes, ceci peut parfois provoquer des mutations aux conséquences plus ou moins graves pour la cellule ou pour l'individu.
Dans l'eau de mer
[modifier | modifier le code]La quantité de potassium dans l'eau de mer est de l'ordre de 0,01 mol/L, soit 1,167 μmol/L de potassium 40. Le calcul réalisé au paragraphe précédent donne donc pour l'eau de mer environ 12,1 Bq/L dus à cet isotope.
Références
[modifier | modifier le code]-
(en) « Live Chart of Nuclides: 40
19K
21 », sur www-nds.iaea.org, AIEA, (consulté le ). - Radioactive Human Body : background radiation - potassium 40 - γ radiation
- Potassium per kilogram fat-free mass and total body potassium: predictions from sex, age, and anthropometry -- Larsson et al. 284 (2): E416 -- AJP - Endocrinology and Metabolism
Annexes
[modifier | modifier le code]Articles connexes
[modifier | modifier le code]- Potassium
- Table des isotopes
- Chaîne de désintégration
- Datation par le potassium-argon
- Calcium 40
- Argon
- Radioactivité
- Dose équivalente en banane
Lien externe
[modifier | modifier le code]- [PDF] (en) Potassium-40, sur le site de l'Argonne National Laboratory
| 1 | H | He | ||||||||||||||||||||||||||||||
| 2 | Li | Be | B | C | N | O | F | Ne | ||||||||||||||||||||||||
| 3 | Na | Mg | Al | Si | P | S | Cl | Ar | ||||||||||||||||||||||||
| 4 | K | Ca | Sc | Ti | V | Cr | Mn | Fe | Co | Ni | Cu | Zn | Ga | Ge | As | Se | Br | Kr | ||||||||||||||
| 5 | Rb | Sr | Y | Zr | Nb | Mo | Tc | Ru | Rh | Pd | Ag | Cd | In | Sn | Sb | Te | I | Xe | ||||||||||||||
| 6 | Cs | Ba | La | Ce | Pr | Nd | Pm | Sm | Eu | Gd | Tb | Dy | Ho | Er | Tm | Yb | Lu | Hf | Ta | W | Re | Os | Ir | Pt | Au | Hg | Tl | Pb | Bi | Po | At | Rn |
| 7 | Fr | Ra | Ac | Th | Pa | U | Np | Pu | Am | Cm | Bk | Cf | Es | Fm | Md | No | Lr | Rf | Db | Sg | Bh | Hs | Mt | Ds | Rg | Cn | Nh | Fl | Mc | Lv | Ts | Og |