Phénobarbital
| Phénobarbital | |
| |
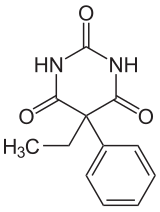
| Structure du phénobarbital | |
| Identification | |
|---|---|
| Nom UICPA | 5-éthyl-5-phj1,3-diazinane-2,4,6-trione |
| No CAS | ; (Na+ sel) |
| No ECHA | 100.000.007 |
| No CE | 200-007-0 200-322-3 (Na) |
| Code ATC | N03 (Antiépileptiques) N05 (Hypnotiques/sédatifs) |
| Propriétés chimiques | |
| Formule | C12H12N2O3 [Isomères] |
| Masse molaire[1] | 232,235 3 ± 0,011 7 g/mol C 62,06 %, H 5,21 %, N 12,06 %, O 20,67 %, |
| Propriétés physiques | |
| T° fusion | 174 à 178 °C[2] |
| Solubilité | < 0,1 g·L-1 dans l'eau à 14 °C[2]
1,2 g·L-1 dans l'eau à 25 °C[3] 2,6 g·L-1 dans l'eau à 45 °C[3] |
| Précautions | |
| Directive 67/548/EEC | |
| Transport | |
| Classification du CIRC | |
| Groupe 2B : Peut être cancérogène pour l'homme[4] | |
| Données pharmacocinétiques | |
| Biodisponibilité | ~ 80 % |
| Liaison protéique | 50 à 60 % |
| Demi-vie d’élim. | 53 - 118 heures en moyenne (jusqu'à 140h chez l'adulte) |
| Excrétion |
urines/selles |
| Considérations thérapeutiques | |
| Voie d’administration | Orale, rectale, parentérale (IM et IV) |
| Caractère psychotrope | |
| Catégorie | Dépresseur hypnotique |
| Mode de consommation |
Ingestion |
| Risque de dépendance | Élevé |
| Unités du SI et CNTP, sauf indication contraire. | |
| modifier |
|
Le phénobarbital est un médicament barbiturique utilisé pour contrôler les convulsions dans certains cas d'épilepsie[5].
Il fut historiquement utilisé pour le traitement des troubles du sommeil, ainsi que comme sédatif afin de soulager les symptômes d'anxiété ou de tension. Il agit en inhibant l'action de neurotransmetteurs excitants dans le système nerveux.
Sa première commercialisation sous les noms Gardénal ou Luminal remonte aux années 1910[6]. Il a été l'un des barbituriques les plus répandus.
Formule chimique
[modifier | modifier le code]La formule chimique du phénobarbital est C12H12N2O3.
Utilisation
[modifier | modifier le code]Très largement prescrit dans les années 1930 et 40 pour traiter des maux divers comme l'épilepsie, il est encore largement prescrit dans le monde chez l'homme, le chien, le chat, les chevaux, les animaux de la ferme, etc.
En France, il n'est plus prescrit que comme traitement anticonvulsivant.
Le produit est répertorié sur la Liste II des substances vénéneuses et n'est disponible que sur ordonnance. Il est inscrit au tableau IV de la Convention sur les substances psychotropes de 1971 ce qui le décrit comme « substance ayant un potentiel d’abus et présentant un risque faible pour la santé publique mais une valeur thérapeutique faible à grande ». En Russie et anciennement en URSS, il est cependant disponible en vente libre et très répandu[7].
Le phénobarbital fait partie de la liste des médicaments essentiels de l'Organisation mondiale de la santé (liste mise à jour en )[8]. Il est aussi utilisé pour traiter le syndrome de Gilbert, ainsi que la maladie de Crigler-Najjar de type II, où il induit une baisse du taux de bilirubine non conjuguée[9].
Mécanisme et durée d'action
[modifier | modifier le code]Contrairement à sa demi-vie d'élimination très longue, le phénobarbital n'agit de façon discernable que durant dix à douze heures[10]. En effet, le facteur limitant de sa durée d'action est davantage sa propension à être dispersé à travers le corps, hors du système nerveux central. On estime son délai d'action à plus d'une heure[10].
Son canal d'action primaire est la modulation positive des récepteurs au GABA de type A[11]. Comme les autres dérivés barbituriques, le phénobarbital potentialise l'action du GABA naturellement produit, tout en agissant aussi comme un agoniste direct de ses récepteurs[12],[13]. Lorsqu'ils sont activés, ces derniers ont un effet inhibiteur sur la stimulation des neurones cibles. Plus spécifiquement l'utilisation d'un barbiturique ouvre davantage le canal ionique Cl- lorsque le GABA (ou un autre agoniste tel que l'alcool[14]) se fixe à ses récepteurs. Cela permet au neurone cible d'absorber encore davantage de charge électriques négatives et réduit son potentiel de stimulation par courant électrique, lorsque des ions positifs tenteront de le charger positivement.
Le barbiturique agit également sur d'autres canaux de manière mineure : on note une action inhibitrice de la recapture de l'adénosine, ainsi qu'un antagonisme des récepteurs AMPA et une inhibition de la sécrétion de glutamate[11],[15].
Comparées aux barbituriques, les benzodiazépines qui les ont largement supplantés, ne sont que des modulateurs positifs de l'action du GABA naturellement produit[16]. Aussi, ils augmentent la fréquence des ouvertures du canal ionique Cl- au lieu d'en augmenter l'amplitude[17]. Ce sont ces diverses différences qui expliquent le caractère plus toxique du phénobarbital comparé à un composé plus moderne.
Effets secondaires
[modifier | modifier le code]Les effets indésirables du produit sont principalement une certaine somnolence, des troubles de la mémoire, des nausées et certaines réactions allergiques cutanées. Ils sont relativement rares, avec une incidence de moins de 10 %[18].
L'ANSM met en garde contre le risque teratogène du phénobarbital : les femmes enceintes sont exposées à un risque trois fois plus grand de malformations du fœtus. Par ailleurs des cas de troubles neurodéveloppementaux sont rapportés[19].
La surdose de ce produit présente cependant un risque élevé de décès[20], en particulier en cas de consommation simultanée d'alcool ou d'autres sédatifs (voire de narcotiques)[21].
Historique et développement
[modifier | modifier le code]
Le premier barbiturique commercialisé fut le barbital, ou acide diéthylbarbiturique (nom commercial: Véronal, tiré du fait qu'il a été inventé en 1903 par Hermann Emil Fischer, chimiste allemand travaillant à Vérone). De nombreux dérivés furent par la suite développés, avec des propriétés plus ou moins spécifiques (solution aqueuse d'action rapide pour le thiopental sodique, capsules hypnotiques puissantes pour le pentobarbital, action longue et progressive pour le phénobarbital) mais un mécanisme d'action toujours similaire.

Lorsque l’on dut trouver un nom pour le phénobarbital (inventé en 1911, dérivé du Véronal), la technique du laboratoire Rhône-Poulenc pour faciliter son introduction et sa mémorisation tant par les médecins que par le public fut de « garder nal de Véronal ». Le nom commercial Gardénal fut donc inventé et est toujours d'actualité[22].
Alors que cette classe de médicaments fut largement détourné pour un usage récréatif jusqu'aux années 1970, le phénobarbital l'était dans une moindre mesure, à cause de son absorption lente et progressive et son action longue. Les produits apparentés à action plus rapide tels que le pentobarbital, amobarbital ou sécobarbital étaient souvent préférés[23] par les toxicomanes et furent impliqués dans des centaines de milliers de cas de dépendance ou de surdose[24].
Suicide de personnalités célèbres
[modifier | modifier le code]- Le , Max Linder s'empoisonne au Gardénal mais est réanimé à temps.
- Le , Marthe Hanau, surnommée « la banquière des années folles », fut retrouvée morte à l'infirmerie de la Prison de Fresnes, d'un « coma toxique » dû à l'absorption d'un tube de Véronal.
- Stefan Zweig, moralement brisé par la Seconde Guerre mondiale, se suicide le en s'empoisonnant au Véronal.
- Pierre Drieu la Rochelle s'est suicidé en ingérant du Gardénal, le .
- le , Margaux Hemingway fut trouvée morte, à la suite d'une surdose de phénobarbital.
Dans la culture populaire
[modifier | modifier le code]- Serge Gainsbourg fait référence au Gardénal dans les chansons Ce mortel ennui (1958) et En relisant ta lettre (1961), Serge Lama dans Les petites femmes de Pigalle (1973), Alain Kan dans Speed My Speed en (1976), Alain Bashung dans L'amour c'est pas confortable (1977), Alain Souchon dans J'ai perdu tout ce que j'aimais (1977) , Hubert-Félix Thiéfaine dans Vendome Gardenal Snack (1980), Daniel Balavoine dans Le blues est blanc (1985), Patricia Kaas dans Mademoiselle chante le blues , Benjamin Biolay dans Jaloux de tout (2009), Oldelaf dans Le monde est beau (2011), Pierre Lapointe dans Zopiclone (2017).
- Dans le film Terminator 3 de Jonathan Mostow (2003), John Connor (Nick Stahl) avale un tube de Phénobarbital qu'il vole dans la pharmacie de la clinique vétérinaire où travaille Kate Brewster (Claire Danes), la future femme du chef de la rébellion et commandante en second de celle-ci.
- Dans le film Ascenseur pour l'échafaud, Véronique (Yori Bertin) et Louis (Georges Poujouly) tentent de se suicider avec du Gardénal.
Notes et références
[modifier | modifier le code]- Masse molaire calculée d’après « Atomic weights of the elements 2007 », sur www.chem.qmul.ac.uk.
- Entrée du numéro CAS « 50-06-6 » dans la base de données de produits chimiques GESTIS de la IFA (organisme allemand responsable de la sécurité et de la santé au travail) (allemand, anglais), accès le 29 novembre 2008 (JavaScript nécessaire).
- (en) David R. Lide, Handbook of chemistry and physics, , 89e éd., chap. 8 (« Aqueous Solubility and Henry’s Law Constants of Organic Compounds »), p. 109.
- IARC Working Group on the Evaluation of Carcinogenic Risks to Humans, « Évaluations globales de la cancérogénicité pour l'Homme, groupe 2B : peut être cancérogène pour l'homme », sur monographs.iarc.fr, CIRC, (consulté le ).
- « Gardénal », sur eurekasante.vidal.fr (consulté le ).
- (en) The Pharmaceutical Journal17 OCT 2012, « Effective, easy to use and affordable — the discovery and use of phenobarbital », sur Pharmaceutical Journal (consulté le ).
- « Corvalol », sur www.chemeurope.com (consulté le ).
- WHO Model List of Essential Medicines, 18th list, avril 2013.
- Philippe Labrune (professeur), « La maladie de Crigler-Najjar », Professeur Jean-Marie Saudubray, Orphanet, 1999, mise à jour 2004 (lire en ligne).
- (en) « Phenobarbital (Phenobarbital): Uses, Dosage, Side Effects, Interactions, Warning », sur RxList (consulté le ).
- (en) Wolfgang Löscher et Michael A. Rogawski, « How theories evolved concerning the mechanism of action of barbiturates », Epilepsia, vol. 53, no s8, , p. 12–25 (ISSN 1528-1167, DOI 10.1111/epi.12025, lire en ligne, consulté le ).
- Yukiko Muroi, Cassandra M. Theusch, Cynthia Czajkowski et Meyer B. Jackson, « Distinct Structural Changes in the GABAA Receptor Elicited by Pentobarbital and GABA », Biophysical Journal, vol. 96, no 2, , p. 499–509 (ISSN 0006-3495, PMID 19167300, PMCID 2716461, DOI 10.1016/j.bpj.2008.09.037, lire en ligne, consulté le ).
- J. M. Rho, S. D. Donevan, M. A. Rogawski, Direct activation of GABAA receptors by barbiturates in cultured rat hippocampal neurons, The Journal of physiology, 497, 1996, (Pt 2): 509–522. PMC 1161000. .
- « LE CERVEAU À TOUS LES NIVEAUX! », sur lecerveau.mcgill.ca (consulté le ).
- Eichi Narimatsu, Tomohisa Niiya, Mikito Kawamata et Akiyoshi Namiki, « [The mechanisms of depression by benzodiazepines, barbiturates and propofol of excitatory synaptic transmissions mediated by adenosine neuromodulation] », Masui. The Japanese Journal of Anesthesiology, vol. 55, no 6, , p. 684–691 (ISSN 0021-4892, PMID 16780077, lire en ligne, consulté le ).
- G. Fillion, « Allostérie et médicaments ».
- Matt T. Bianchi, Emmanuel J. Botzolakis, Andre H. Lagrange et Robert L. Macdonald, « Benzodiazepine modulation of GABA(A) receptor opening frequency depends on activation context: a patch clamp and simulation study », Epilepsy Research, vol. 85, nos 2-3, , p. 212–220 (ISSN 1872-6844, PMID 19447010, PMCID 2834588, DOI 10.1016/j.eplepsyres.2009.03.007, lire en ligne, consulté le ).
- « Notice patient - GARDENAL 100 mg, comprimé - Base de données publique des médicaments », sur base-donnees-publique.medicaments.gouv.fr (consulté le ).
- [PDF] Synthèse du rapport Antiépileptiques au cours de la grossesse : État actuel des connaissances sur le risque de malformation et de troubles neuro-développementaux, .
- Jolee T. Suddock et Matthew D. Cain, « Barbiturate Toxicity », dans StatPearls, StatPearls Publishing, (PMID 29763050, lire en ligne).
- (en-US) « Phenobarbital Overdose », sur Alta Mira Recovery (consulté le ).
- Étymologie de Gardénal d'après le Centre national de ressources textuelles et lexicales, citant Rob. Suppl. et Cah. de l'Assoc. internat. des ét. fr., mai 1973, no 25, p. 321.
- (en-GB) Andrew M. Brown, « Winston Churchill's drinking was one thing, but what about his drug-taking? », The Daily Telegraph, (ISSN 0307-1235, lire en ligne, consulté le ).
- Francisco López-Muñoz, Ronaldo Ucha-Udabe et Cecilio Alamo, « The history of barbiturates a century after their clinical introduction », Neuropsychiatric Disease and Treatment, vol. 1, no 4, , p. 329–343 (ISSN 1176-6328, PMID 18568113, PMCID 2424120, lire en ligne, consulté le ).
Voir aussi
[modifier | modifier le code]Article connexe
[modifier | modifier le code]Lien externe
[modifier | modifier le code]- Compendium suisse des médicaments : spécialités contenant Phénobarbital


