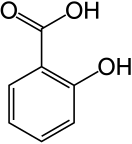
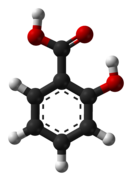
Салици́ловая кислота́ (от лат. salix «ива», из коры которой она была впервые выделена) — низкомолекулярное органическое соединение, 2-гидроксибензойная или фенольная кислота. Бесцветные кристаллы, хорошо растворима в этаноле, диэтиловом эфире и других полярных органических растворителях, плохо растворима в воде (1,8 г/л при +20 °C).
| Салициловая кислота | |||
|---|---|---|---|
| |||
| Общие | |||
| Систематическое наименование |
2-гидроксибензойная кислота | ||
| Традиционные названия | Салициловая кислота | ||
| Хим. формула | C7H6O3 | ||
| Физические свойства | |||
| Состояние | твёрдое | ||
| Молярная масса | 138,12 г/моль | ||
| Плотность | 1,44 г/см³ | ||
| Термические свойства | |||
| Температура | |||
| • плавления | 159 °C | ||
| • кипения | 211 °C | ||
| Химические свойства | |||
| Константа диссоциации кислоты |
1 = 2,97 (+25 °C) 2 = 13,82 (+20 °C) |
||
| Растворимость | |||
| • в воде | 0,2 г/100 мл | ||
| Классификация | |||
| Рег. номер CAS | 69-72-7 | ||
| PubChem | 338 и 118212070 | ||
| Рег. номер EINECS | 200-712-3 | ||
| SMILES | |||
| InChI | |||
| RTECS | VO0525000 | ||
| ChEBI | 16914 | ||
| ChemSpider | 331 | ||
| Безопасность | |||
| NFPA 704 | |||
| Приведены данные для стандартных условий (25 °C, 100 кПа), если не указано иное. | |||
Выделена из ивовой коры итальянским химиком Рафаэлем Пириа и затем синтезирована им же.
Распространение в природе
правитьВ природе встречается в растениях в виде производных — главным образом в виде гликозида метилового эфира (в частности, салициловая кислота была впервые выделена из коры ивы, откуда и происходит название), свободная салициловая кислота наряду с салициловым альдегидом в небольших количествах содержится в эфирном масле, выделяемых из цветов некоторых видов спиреи (Spiraea ulmaria, Spiraea digitata).
Синтез
правитьСалициловую кислоту получают по реакции Кольбе — Шмитта из фенолята натрия и углекислого газа в автоклавах при 180 °С с последующей обработкой продукта реакции соляной кислотой:
Физические свойства
правитьСалициловая кислота легкорастворима в этаноле, диэтиловом эфире, малорастворима в сероуглероде. Растворимость в воде (г/л): 1,2 (0 °C), 1,8 (20 °C), 8,2 (60 °C), 20,5 (80 °C).
Химические свойства
правитьЯвляется двухосновной кислотой (очень слабой по второй ступени): pK1 = 2,97 pK2 = 13.82.
Реакционная способность бензольного ядра салициловой кислоты определяется наличием двух заместителей с противоположными мезомерным и индуктивным эффектами: донорной гидроксильной и акцепторной карбоксильной: в результате салициловая кислота значительно легче бензойной, но не так активно, как фенол, вступает в реакции электрофильного замещения вследствие стабилизации промежуточного σ-комплекса гидроксильной группой.
Электрофильное замещение направляется в орто- и пара-положения к гидроксилу и зачастую сопровождается декарбоксилированием: так, нитрование салициловой кислоты приводит к пикриновой кислоте (2,4,6-тринитрофенолу), а бромирование — к 2,4,6-трибромфенолу, хотя сульфирование олеумом идёт без декарбоксилирования и даёт сульфосалициловую (2-гидрокси-5-сульфобензойную) кислоту.
При нагревании салициловая кислота декарбоксилируется до фенола, в промышленности салициловую кислоту обычно получают обратной реакцией — карбоксилированием фенолята натрия углекислым газом при 150—180 °C и давлении 5 атм (реакция Кольбе — Шмитта):
Следует обратить внимание, что такое карбоксилирование фенола, во-первых обратимо и, во-вторых, существенную роль в карбоксилировании в орто-положение к фенольному гидроксилу играет эффект взаимодействия координационной связи катиона щелочного металла с кислородными лигандами с образованием хелатообразного промежуточного состояния: так, в орто-положение с образованием салицилата карбоксилирование происходит только в случае фенолятов натрия и лития, в случае фенолятов калия, рубидия и цезия карбоксилирование идёт по пара-положению — катионы этих щелочных металлов имеют больший радиус и координационная стабилизация переходного состояния невозможна. Об обратимости реакции говорит также перегруппировка дикалиевой соли салициловой кислоты в дикалиевую соль пара-гидроксибензойной кислоты и превращение натриевой соли пара-гидроксибензойной кислоты при нагревании в динатриевую соль салициловой кислоты.
Такое хелатообразование характерно для салициловой кислоты — так, качественный метод обнаружения салициловой кислоты основан на образовании интенсивно окрашенных в сине-фиолетовый цвет комплексов с хлоридом железа(III).
Каталитическое гидрирование на платине, а также восстановление натрием в изоамиловом спирте ведёт к пимелиновой кислоте HOOC(CH2)5COOH.
Салицилаты
правитьСалициловая кислота образует соли — салицилаты. Некоторые представители:
Физиологическая роль и действие салицилатов
правитьДействие на человека и животных
правитьСалициловая кислота и салицилаты, а также её сложные эфиры (метилсалицилат) и другие синтетические производные салициловой кислоты (например, ацетилсалициловая кислота — аспирин), обладают выраженным противовоспалительным действием.
Гормон растений
правитьПоказано действие салициловой кислоты как фитогормона. Салициловая кислота вызывает повышение температуры в отдельных органах термогенных растений (в частности, у некоторых представителей семейства Ароидных). Это происходит по причине разрыва транспорта электронов в митохондриальной дыхательной цепи. Активно изучается роль салициловой кислоты в развитии неспецифической реакции на стрессогенные факторы и накопление в клетках активных форм кислорода.
Применение салициловой кислоты
правитьПрименение в медицине
правитьСалициловая кислота — активный компонент ивовой коры. Ещё в XIX в. её использовали для лечения ревматизма и мочекислого диатеза, а сегодня это вещество синтезируют в больших количествах, так как оно служит основой для производства многих лекарств.
Салициловая кислота обладает слабыми антисептическими, раздражающими и кератолитическими (в больших концентрациях) свойствами и применяется в медицине наружно в мазях и растворах при лечении кожных заболеваний; входит в состав пасты Лассара, присыпки «гальманин», препаратов «мозольная жидкость» и «мозольный пластырь». В аптечной сети продаётся в таких лекарственных формах, как спиртовой раствор для наружного применения, известный в народе как «салициловый спирт» (с содержанием салициловой кислоты 1 или 2 %) и мазь (2-, 3-, 5- и 10-процентная).[1]
Производные салициловой кислоты также применяются в медицине: амид (салициламид) и уксуснокислый эфир (ацетилсалициловая кислота) используют как жаропонижающие, противоревматические, противовоспалительные и болеутоляющие средства; фенилсалицилат — как антисептик; пара-аминосалициловую кислоту (структурно близкую с пара-аминобензойной кислотой, необходимой туберкулезным микобактериям, и поэтому метаболически конкурирующую с ней) — как специфическое противотуберкулёзное средство.
Другие сферы применения
правитьТоксические свойства и требования безопасности
правитьСалициловая кислота токсична в больших дозах, для человека предполагаемая LD50 составляет 1,75 г/кг[3]. Беременным советуют не употреблять продуктов, содержащих салицилаты, из-за повышения риска развития синдрома Рея.
В организме человека салициловая кислота метаболизируется, образуя конъюгаты с глюкуроновой кислотой (о-гидроксибензоилглюкуронид и о-карбоксифенилглюкуронид) и глицином, либо путём гидроксилирования до 2,3- и 2,5-дигидроксибензойной и 2,3,5-тригидроксибензойной кислот. Салициловая кислота и её метаболиты выводятся из организма с мочой[4].
Примечания
править- ↑ Поиск по базе данных ЛС, опции поиска: МНН — Салициловая кислота, флаги «Искать в реестре зарегистрированных ЛС», «Искать ТКФС», «Показывать лекформы». Обращение лекарственных средств. ФГУ «Научный центр экспертизы средств медицинского применения» Росздравнадзора РФ (23 августа 2010). Дата обращения: 11 января 2012. Архивировано из оригинала 3 сентября 2011 года.
- ↑ Химическая энциклопедия : в 5 т. / Гл. ред.: И. Л. Кнунянц (Т. 1—3), Н. С. Зефиров (Т. 4—5). — М.: Советская энциклопедия (Т. 1—2); Большая Российская энциклопедия (Т. 3—5), 1988—1998. — ISBN 5-85270-008-8.
- ↑ Safety data for acetylsalicylic acid // MSDS. Дата обращения: 17 сентября 2009. Архивировано из оригинала 16 июля 2011 года.
- ↑ В. Ф. Крамаренко. Токсикологическая химия. — К.: Выща шк., 1989. — 447 с. — 6000 экз. — ISBN 5-11-000148-0.
Литература
править- I. Raskin Role of Salicylic Acid in Plants. Annual Review of Plant Physiology and Plant Molecular Biology, June 1992, Vol. 43, Pages 439—463
- Курц А. Л., Ливанцов М. В., Ливанцова Л. И. Фенолы и хиноны.
- Salicylic Acid — A Plant Hormone. Hayat, S.; Ahmad, A. (Eds.) 2007, Approx. 400 p., Springer, Berlin, Hardcover
- Vlot A.C. Dempsey D.A., Klessig D.F. Salicylic Acid, a Multifaceted Hormone to Combat Disease // Annu. Rev. Phytopathol. 2009. 47: 177—206.
- Глава «Салициловая кислота» из книги «Жаропонижающие», Нотнагель Г., 1902 год, стр. 28