Hexafluorure d'osmium
Apparence
| Hexafluorure d'osmium | |
| |
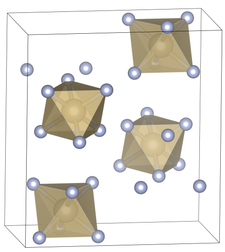
| __ Os6+ __ F− Structure cristalline du fluorure d'osmium(VI) |
|
| Identification | |
|---|---|
| Nom UICPA | hexafluoroosmium |
| Synonymes |
fluorure d'osmium(VI) |
| No CAS | |
| No ECHA | 100.033.969 |
| No CE | 237-382-5 |
| PubChem | 123327 |
| SMILES | |
| InChI | |
| Apparence | solide jaune cristallisé[1] |
| Propriétés chimiques | |
| Formule | OsF6 |
| Masse molaire[2] | 304,22 ± 0,03 g/mol F 37,47 %, Os 62,53 %, |
| Propriétés physiques | |
| T° fusion | 33,4 °C[1] |
| T° ébullition | 47,5 °C[1] |
| Masse volumique | 5,09 g/cm3[3] à −140 °C |
| Cristallographie | |
| Système cristallin | orthorhombique[3] |
| Classe cristalline ou groupe d’espace | Pnma (no 62) [3] |
| Paramètres de maille | a = 938,7 pm, b = 854,3 pm, c = 494,4 pm, Z = 4[3] |
| Unités du SI et CNTP, sauf indication contraire. | |
| modifier |
|
L'hexafluorure d'osmium, ou fluorure d'osmium(VI), est un composé chimique de formule OsF6. Il se présente sous la forme d'un solide jaune cristallisé dans le système orthorhombique selon le groupe d'espace Pnma (no 62) avec les paramètres cristallins a = 938,7 pm, b = 854,3 pm, c = 494,4 pm et quatre atomes d'osmium par maille cristalline donnant une masse volumique calculée de 5,09 g/cm3[3]. Il fond à 33,4 °C et bout à 47,5 °C[1]. La molécule OsF6 a une symétrie Oh correspondant à une géométrie ocatédrique, avec des liaisons Os–F longues de 182,7 pm[3].
On peut obtenir l'hexafluorure d'osmium en faisant réagir de l'osmium avec un excès de fluor F2 à 300 °C[3] :
Notes et références
[modifier | modifier le code]- (en) David R. Lide, « Properties of the Elements and Inorganic Compounds », CRC Handbook of Chemistry and Physics, 90e éd., CRC Press/Taylor and Francis, 2009, p. 4-79. (ISBN 978-1-4200-9084-0)
- Masse molaire calculée d’après « Atomic weights of the elements 2007 », sur www.chem.qmul.ac.uk.
- (en) Thomas Drews, Joanna Supeł, Adelheid Hagenbach et Konrad Seppelt, « Solid State Molecular Structures of Transition Metal Hexafluorides », Inorganic Chemistry, vol. 45, no 9, , p. 3782-3788 (PMID 16634614, DOI 10.1021/ic052029f, lire en ligne)



