Sülfat: Revizyonlar arasındaki fark
Görünüm
| [kontrol edilmemiş revizyon] | [kontrol edilmiş revizyon] |
İçerik silindi İçerik eklendi
123335229778553657 Etiketler: Elle geri alma Geri alındı |
Değişiklik özeti yok Etiketler: Geri al Mobil değişiklik Mobil ağ değişikliği Gelişmiş mobil değişikliği |
||
| 96. satır: | 96. satır: | ||
| PEL = }} |
| PEL = }} |
||
}} |
}} |
||
'''Sülfat iyonu,''' [[inorganik kimya]]da bir [[ |
'''Sülfat iyonu,''' [[inorganik kimya]]da bir [[]] atomu ile bunu tetrahedral yapıda çevreleyen dört eş oksijen atomundan oluşan, negatif yüklü bir anyondur. [[:wikt:ampirik|Ampirik]] formülü [[sülfür|S]][[oksijen|O]]<sub>4</sub><sup>2-</sup> ve moleküler ağırlığı 96,06 [[dalton]]dur. Hidrojenle birleştiğinde [[sülfürik asit]] oluşturur. Ayrıca,[[Dimetil sülfat]] gibi organik sülfatlar, kovalent bileşiklerdir ve sülfürik asidin [[ester]]leridir. |
||
* [[Sülfürik asit]]te metalin eritilmesi |
* [[Sülfürik asit]]te metalin eritilmesi |
||
Sayfanın 14.36, 22 Haziran 2024 tarihindeki hâli
Bu madde hiçbir kaynak içermemektedir. (Nisan 2016) (Bu şablonun nasıl ve ne zaman kaldırılması gerektiğini öğrenin) |

| |
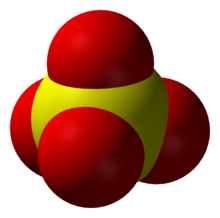
| |
| Adlandırmalar | |
|---|---|
Sülfat | |
| Tanımlayıcılar | |
3D model (JSmol)
|
|
| ChEBI | |
| ChemSpider | |
| ECHA InfoCard | 100.108.048 |
| EC Numarası |
|
PubChem CID
|
|
CompTox Bilgi Panosu (EPA)
|
|
| |
| |
| Özellikler | |
| Molekül formülü | SO42- |
| Molekül kütlesi | 96.06 g/mol |
| Aksi belirtilmediği sürece madde verileri, Standart sıcaklık ve basınç koşullarında belirtilir (25 °C [77 °F], 100 kPa).
| |
| Bilgi kutusu kaynakları | |
Sülfat iyonu, inorganik kimyada bir sülfür atomu ile bunu tetrahedral yapıda çevreleyen dört eş oksijen atomundan oluşan, negatif yüklü bir anyondur. Ampirik formülü SO42- ve moleküler ağırlığı 96,06 daltondur. Hidrojenle birleştiğinde sülfürik asit oluşturur. Ayrıca,Dimetil sülfat gibi organik sülfatlar, kovalent bileşiklerdir ve sülfürik asidin esterleridir.
- Sülfürik asitte metalin eritilmesi
- Sülfürik asidin bir metal hidroksit veya oksit ile reaksiyonu
- Metal sülfür veya sülfitlerin oksidasyonu
Hidrojen sülfat
Sülfürik asit ile suyun tepkimeye girmesiyle iki hidrojen sülfat ve hidronyum oluşur. Yapısında bir hidrojen, bir kükürt ve dört oksijen bulunur. İyon yükü ise anyondur.
Kaynakça
| İnorganik kimya ile ilgili bu madde taslak seviyesindedir. Madde içeriğini genişleterek Vikipedi'ye katkı sağlayabilirsiniz. |
