Železov(III) oksid
| |

| |
| Imena | |
|---|---|
| IUPAC ime
Iron(III) oxide
| |
| Druga imena | |
| Identifikatorji | |
3D model (JSmol)
|
|
| ChEBI | |
| ChemSpider | |
| ECHA InfoCard | 100.013.790 |
| Število E | E172(ii) (barvila) |
| KEGG | |
PubChem CID
|
|
| RTECS število |
|
| UNII | |
CompTox Dashboard (EPA)
|
|
| |
| |
| Lastnosti | |
| Fe2O3 | |
| Molska masa | 159,69 g·mol−1 |
| Videz | rdečerjava trdnina |
| Vonj | brez vonja |
| Gostota | 5,242 g/cm3[1] |
| Tališče | 1.539–1.565 °C (2.802–2.849 °F; 1.812–1.838 K) |
| netopen | |
| Topnost | topen v razredčenih kislinah,[2] raztopini sladkorja, trihidrat rahlo topen v vodnih raztopinah vinske, citronske in ocetne kisline[3] |
| Struktura | |
| Kristalna struktura | romboedrična,[4] Pearsonov simbol hR30 (α-oblika), kubična biksbiitska, cI80 (β-oblika), kubična spielska (γ-oblika), ortorombska (ε-oblika)[5] |
| Prostorska skupina | R3c, No. 161 (α-oblika)[4] Ia3, No. 206 (β-oblika) Pna21, No. 33 (ε-oblika)[5] |
| 3m (α-oblika)[4] 2/m 3 (β-oblika) mm2 (ε-oblika)[5] | |
| Koordinacijska geometrija |
oktaedrična (Fe3+, α-oblika, β-oblika) |
| Termokemija | |
| Specifična toplota, C | 103,9 J/mol·K[2] |
| Standardna molarna entropija S |
87,4 J/mol·K[2] |
Std tvorbena
entalpija (ΔfH⦵298) |
−824,2 kJ/mol[2] |
Gibbsova prosta energija (ΔfG˚)
|
−742,2 kJ/mol[2] |
| Nevarnosti | |
| GHS piktogrami |  [6] [6]
|
| Opozorilna beseda | Nevarno |
| H315, H319, H335[6] | |
| P261, P305+351+338[6] | |
| NFPA 704 (diamant ognja) | |
| 5 mg/m3 (TWA) | |
| Smrtni odmerek ali koncentracija (LD, LC): | |
LD50 (srednji odmerek)
|
10 g/kg (podgana, oralno) |
| Sorodne snovi | |
| Drugi anioni | železov(III) fluorid |
| Drugi kationi | manganov(III) oksid kobaltov(III) oksid |
| Sorodno železovi oksidi | železov(II) oksid železov(II,III) oksid |
Če ni navedeno drugače, podatki veljajo za material v standardnem stanju pri 25 °C, 100 kPa). | |
| Sklici infopolja | |
Železov(III) oksid je anorganska spojina s formulo Fe2O3. Je eden od treh glavnih železovih oksidov. Druga dva sta železov(II) oksid (FeO), ki je redek, in železov(II,III) oksid (Fe3O4), ki se v naravi pojavlja tudi kot mineral magnetit. Mineral železovega(III) oksida je hematit, ki je glavni vir železa za jeklarsko industrijo. Fe2O3 je feromagneten, temno rdeč mineral, topen v kislinah. Pogosto se imenuje tudi rja, ki ima podobno sestavo in lastnosti kot hematit. Rja je slabo definirana snov, opisana kot hidrirani železovi oksidi.
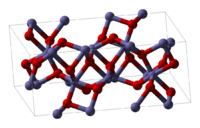
Zgradba
[uredi | uredi kodo]Fe2O3 ima več polimorfov. Prevladujeta polimorfa α in γ, ki imata oktaedrsko geometrijo, v kateri je na centralni Fe atom vezanih šest kisikovih ligandov.
α-Fe2O3
[uredi | uredi kodo]α-Fe2O3 ima romboedrsko zgradbo korunda (α-Al2O3) in je najpogostejša oblika železovega(III) oksida. V naravi se pojavlja kot mineral hematit, ki je hkrati tudi najpomembnejša železova ruda. Hematit je pod približno 260 K antiferomagneten (Morinov prehod). Pri temperaturah med 260 in 950 K je šibko feromagneten (Néelova temperatura).[7] Magnetne lastnosti so odvisne od več dejavnikov, kot so tlak, velikost delcev in jakost magnetnega polja.
γ-Fe2O3
[uredi | uredi kodo]γ-Fe2O3 ima kubično zgradbo. Je metastabilen in nastaja pri visokih temperaturah iz α-Fe2O3. V naravi se pojavlja kot mineral maghemit. Je feromagneten in se uporablja na primer v magnetofonskih trakovih.[8] Ultrafini delci, manjši od 10 nm, so superparamagnetni. Pripravi se lahko s termično dehidracijo γ-železovega(III) oksida-hidroksida ali s previdno oksidacijo železovega(II,III) oksida.[8] Ultrafini delci se lahko pripravijo s termičnim razpadom železovega(III) oksalata.
Drugi polimorfi
[uredi | uredi kodo]Železov(III) oksid ima tudi več drugih polimorfov. β-polimorf je telesno centrirana kocka (prostorska skupina Ia3), ki pri temperaturi nad 500 °C preide v α-Fe2O3. Pripravi se lahko z redukcijo hematita z ogljikom, pirolizo raztopine železovega(III) klorida ali termičnim razpadom železovega(III) sulfata.
ε-Fe2O3 je rombski in ima lastnosti med α in γ-polimorfom. ε-Fe2O3 ima uporabne magnetne lastnosti. Priprava čistega ε-Fe2O3 je zelo težavna zaradi onesnaženja z α in γ-polimorfoma. Dokaj čist ε-Fe2O3 se lahko pripravi s termično pretvorbo γ-polimorfa. Tudi ta polimorf je metastabilen in pri temperaturi 500-750 °C preide v α-Fe2O3. Pripravi se lahko tudi z oksidacijo železa v električnem oboku ali s sol-gel precipitacijo železovega(III) nitrata.
Nedavne raziskave so odkrile prisotnost ε-Fe2O3 v glazurah stare kitajske keramike.[9]
Pri visokih tlakih obstaja tudi amorfna oblika železovega(III) oksida.[5]
Hidrirani železovi(III) oksidi
[uredi | uredi kodo]Obstaja več hidriranih železovih(III) oksidov. Če se topnim železovim(III) solem dodajo alkalije, nastane rdečerjava želatinasta oborina, ki ni Fe(OH)3, ampak Fe2O3•H2O (piše se tudi kot Fe(O)OH). Obstaja tudi več oblik hidriranega železovega(III) oksida. Rdeči lepidokrocit, ki nastane na zunanji površini stalaktitom podobnih tvorb, je γ-Fe(O)OH. V njihovi notranjosti se pojavlja oranžni getit. Fe2O3•H2O med segrevanjem izgubi vezano vodo. S segrevanjem na 1.670 K se Fe2O3 pretvori v črn Fe3O4 (Fe(II)Fe(III)2O4), ki je znan kot mineral magnetit. Fe(O)OH je topen v kislinah, pri čemer nastane [Fe(OH2)6]3+. V koncentriranih alkalijah se Fe2O3 pretvori v [Fe(OH)6]3−.[8]
Reakcije
[uredi | uredi kodo]Najpomembnejša reakcija je redukcija z ogljikom, v kateri nastane elementarno železo:
- 2 Fe2O3 + 3 C → 4 Fe + 3 CO2
Druga je ekstremno eksotermna termitska reakcija z aluminijem:[10]
- 2 Al + Fe2O3 → 2 Fe + Al2O3
Reakcija je uporabna za varjenje debelih železnih predmetov, na primer železniških tirnic. Termit se uporablja tudi kot orožje in sredstvo za izdelavo majhnih ulitih kovinskih predmetov in orodij.
Z delno redukcijo z vodikom pri približno 400 °C nastane magnetit, ki je zmes železovega(II) in (III) oksida:[11]
- 3 Fe2O3 + H2 → 2 Fe3O4 + H2O
Železov(III) oksid je netopen v vodi. Topen je v močnih kislinah, na primer v klorovodikovi iz žveplovi kislini. Topen je tudi v raztopinah kelatov, na primer EDTA, in oksalni kislini.
S segrevanjem železovih(III) oksidov z drugimi kovinskimi oksidi in karbonati nastanejo ferati:[11]
- ZnO + Fe2O3 → Zn(FeO2)2
Priprava
[uredi | uredi kodo]Železov(III) oksid se v laboratoriju lahko pripravi z elektrolizo raztopine natrijevega bikarbonata z železno anodo:
- 4 Fe + 3 O2 + 2 H2O → 4 FeO(OH)
Nastali hidrirani železov(III) oksid (FeO(OH)) pri približno 200 °C odcepi vezano vodo:[11][12]
- 2 FeO(OH) → Fe2O3 + H2O
Pripravi se lahko tudi s termičnim razpadom železovega(III) hidroksida pri temperaturah nad 200 °C:
- 2 Fe(OH)3 → Fe2O3 + 3H2O
Uporaba
[uredi | uredi kodo]Železov(III) oksid je glavna surovina za proizvodnjo železa, jekla in mnogo drugih zlitin.[12]
Polirno sredstvo
[uredi | uredi kodo]Zelo drobno uprašen železov(III) oksid se uporablja za končno poliranje kovinskega nakita in optičnih leč. Zlatarji odstranjujejo ostanke oksida z nakita z izpiranjem v ultrazvočni kopeli.
Pigment
[uredi | uredi kodo]Železov(III) oksid se uporablja tudi kot pigment s tržnimi imeni »rjavi pigment 6«, »rjavi pigment 7« in »rdeči pigment 101«.[13] Pigmenta rdeče 101 in rjavo 6 se lahko uporabljata tudi v kozmetiki. Železovi oksidi se kot pigmenti skupaj s titanovimi oksidi uporabljajo v zobni protetiki.[14]
Hematit je značilna komponenta švedsko rdeče barve, znane tudi kot falunska rdeča barva.
Magnetni spominski mediji
[uredi | uredi kodo]Železov(III) oksid je najpogostejši magnetni delec v vseh vrstah medijev za zapisovanje in shranjevanje podatkov. Sodobni mediji, predvsem trdi diski, uporabljajo bolj dodelane tehnologije, v katerih so premazi sestavljeni iz 15 slojev ali celo več.[15]
Fotokatalizator
[uredi | uredi kodo]α-Fe2O3 se že več kor 25 let preučuje kot fotoanoda za reakcijo razgradnjo vode v kisik in vodik.[16]
Medicina
[uredi | uredi kodo]Zmes cinkovega oksida in približno 0,5 % železovega(III) oksida se imenuje calamine in je aktivna komponenta kalaminskega losjona.
Sklici
[uredi | uredi kodo]- ↑ 1,0 1,1 SDS of Iron(III) oxide. Kurt J Lesker Company Ltd., Anglija. 5. januar 2012. Pridobljeno 12. julija 2014.
- ↑ 2,0 2,1 2,2 2,3 2,4 D.R. Lide, urednik (2009). CRC Handbook of Chemistry and Physics. 90. izdaja. Boca Raton, Florida: CRC Press. ISBN 978-1-4200-9084-0.
- ↑ 3,0 3,1 A.M. Comey, D.A. Hahn (1921). A Dictionary of Chemical Solubilities: Inorganic. 2. izdaja. New York: The MacMillan Company. str. 433.
- ↑ 4,0 4,1 4,2 Y. Ling, D.A. Wheeler, J.Z. Zhang, Y. Li (2013). One-Dimensional Nanostructures: Principles and Applications. http://www.wiley.com . Hoboken, New Jersey: John Wiley & Sons, Inc.. str. 167. ISBN 978-1-118-07191-5.
- ↑ 5,0 5,1 5,2 5,3 M. Vujtek, R. Zboril, R. Kubinek, M. Mashlan. Ultrafine Particles of Iron(III) Oxides by View of AFM – Novel Route for Study of Polymorphism in Nano-world. http://atmilab.upol.cz. Pridobljeno 12. julija 2014.
- ↑ 6,0 6,1 6,2 Sigma-Aldrich Co., Iron(III) oxide. Pridobljeno 12. julija 2014.
- ↑ J.E. Greedon (1994). Magnetic oxides. Encyclopedia of Inorganic chemistry. New York: John Wiley & Sons. ISBN 0-471-93620-0.
- ↑ 8,0 8,1 8,2 C.E. Housecroft, A.G. Sharpe (2008). Chapter 22: d-block metal chemistry: the first row elements. Inorganic Chemistry. 3. izdaja. Pearson. str. 716. ISBN 978-0-13-175553-6.
- ↑ C. Dejoie, P. Sciau, W. Li, L. Noé, A. Mehta, K. Chen, H. Luo, M. Kunz, N. Tamura, Z. Liu. Learning from the past: Rare ε-Fe2O3 in the ancient black-glazed Jian (Tenmoku) wares. Scientific Reports 4. Article number: 4941. doi: 10.1038/srep04941 Pridobljeno 20. februarja 2014.
- ↑ A. Price (1945). Higher School Certificate Inorganic Chemistry. Leslie Slater Price.
- ↑ 11,0 11,1 11,2 Handbook of Preparative Inorganic Chemistry. 2. izdaja. Academic Press. 1963. NY. Vol. 1, str. 1661.
- ↑ 12,0 12,1 N.N. Greenwood; A. Earnshaw (1997). Chemistry of the Elements (2 izd.). Oxford [etc.] : Butterworth Heinemann. COBISS 18882053. ISBN 0-7506-3365-4.
- ↑ Paint and Surface Coatings: Theory and Practice. William Andrew Inc. ISBN 1-884207-73-1.
- ↑ A. Banerjee (2011). Pickard's Manual of Operative Dentistry. United States: Oxford University Press Inc., New York. str. 89. ISBN 978-0-19-957915-0.
- ↑ S.N. Piramanayagam. Perpendicular recording media for hard disk drives. J. Appl. Phys. 102, 011301 (2007).
- ↑ A. Kay, I. Cesar, M. Gratzel (2006). Journal of the American Chemical Society 128: 15714-15721.



