Hypoxanthine
| Hypoxanthine | ||||
|---|---|---|---|---|
| Structuurformule en molecuulmodel | ||||
| ||||
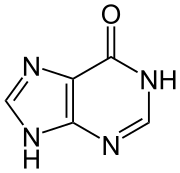
Structuurformule van hypoxanthine
| ||||
| Algemeen | ||||
| Molecuulformule | C5H4N4O | |||
| IUPAC-naam | 1H-purin-6(9H)-one | |||
| Andere namen | 6-hydroxypurine | |||
| Molmassa | 136,11 g/mol | |||
| CAS-nummer | 68-94-0 | |||
| PubChem | 790 | |||
| Wikidata | Q410305 | |||
| Fysische eigenschappen | ||||
| Aggregatietoestand | vast | |||
| Smeltpunt | > 300 °C | |||
| Tenzij anders vermeld zijn standaardomstandigheden gebruikt (298,15 K of 25 °C, 1 bar). | ||||
| ||||
Hypoxanthine is een natuurlijk voorkomend derivaat van purine. Het is een intermediaire verbinding in de stofwisselingsroutes van purines. Hypoxanthine kan als 'afwijkende base' voorkomen in nucleïnezuren. Het is bijvoorbeeld aanwezig in het anticodon van tRNA in de vorm van zijn nucleoside inosine.
Hypoxanthine wordt in de microbiologie gebruikt als additief in bepaalde cel-, bacterie- en parasietculturen. Het fungeert als substraat en als stikstofbron. Het is bijvoorbeeld een vereist reagens in malariaculturen; de ziekteverwekker Plasmodium falciparum heeft hypoxanthine nodig voor zijn nucleïnezuursynthese en energiemetabolisme.[1]
Reacties
[bewerken | brontekst bewerken]Hypoxanthine kan onder invloed van xanthine-oxidase worden omgezet in xanthine. Deze reactie is reversibel, maar bij de afbraak van purine in natuurlijke situatie wordt xanthine uit hypoxanthine gevormd (xanthine zal vervolgens vaak in urinezuur worden omgezet). Hypoxanthine is daarnaast een substraat dat gebruikt wordt tijdens salvage van nucleotiden voor omzetting in IMP.[2]
Hypoxanthine wordt in cellen soms spontaan gevormd door deaminering van adenine. Vanwege de gelijkenis met guanine (hypoxanthine kan basenparen met cytosine), kan deze deaminering van adenine leiden tot een fout in de transcriptie of replicatie van DNA. Hypoxanthine wordt uit het DNA verwijderd door gespecialiseerde reparatie-eiwitten.[3][4]
Zie ook
[bewerken | brontekst bewerken]Bronnen
- ↑ (en) Denise L. Doolan (2002). Malaria Methods and Protocols. Springer Science & Business Media, p. 484. ISBN 978-1-59259-271-5.
- ↑ (en) Berg, J. (2015). Biochemistry, 8th edition. W. H. Freeman and Company, New York, 752. ISBN 978-1-4641-2610-9.
- ↑ (en) Lee, Chun-Yue (2009). Recognition and Processing of a New Repertoire of DNA Substrates by Human 3-Methyladenine DNA Glycosylase (AAG). Biochemistry 10: 1850-1861. PMID 19219989. PMC 2883313. DOI: 10.1021/bi8018898.
- ↑ (en) Alberts, B. Johnson, A. Lewis, J. (2015). Molecular Biology of The Cell, 6th edition. Garland Science, pp. 271-272. ISBN 978-0-8153-4464-3.
