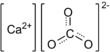Kalsiyum karbonat
Kalsiyum karbonat, halk arasında kireç taşı olarak bilinen bir tür kimyasal bileşiktir. Bileşik formülü CaCO3 şeklindedir. Bu bileşik doğada en fazla eski kayaçlarda ve deniz kabuklarında bulunur. Kalsiyum karbonat, antiasitlerin bir üyesi olsa da, fazlası biyolojik olarak zararlıdır.
| |||

| |||
| Adlandırmalar | |||
|---|---|---|---|
Kalsiyum karbonat | |||
| Tanımlayıcılar | |||
3D model (JSmol)
|
|||
| ChEBI | |||
| ChEMBL | |||
| ChemSpider | |||
| ECHA InfoCard | 100.006.765 | ||
| EC Numarası |
| ||
| E numaraları | E170 (renkler) | ||
| KEGG | |||
PubChem CID
|
|||
| RTECS numarası |
| ||
| UNII | |||
CompTox Bilgi Panosu (EPA)
|
|||
| |||
| |||
| Özellikler | |||
| Molekül formülü | CaCO3 | ||
| Molekül kütlesi | 100,0869 gr/mol | ||
| Görünüm | İnce beyaz toz; tebeşir tadında | ||
| Koku | kokusuz | ||
| Yoğunluk | 2,711 gr/cm³ (kalsit) 2,83 gr/cm³ (aragonit) | ||
| Erime noktası | 1.339 °C (2.442 °F; 1.612 K) (kalsit) 825 °C (1.517 °F; 1.098 K) (aragonit)[3] | ||
| Kaynama noktası | parçalanır | ||
| Çözünürlük (su içinde) | 0,013 gr/L (25 °C)[1][2] | ||
| Çözünürlük (seyreltik asitler içinde) | çözünür | ||
| Asitlik (pKa) | 9,0 | ||
| Kırınım dizimi (nD) | 1,59 | ||
| Yapı | |||
| Trigonal | |||
| 32/m | |||
| Termokimya | |||
Standart molar entropi (S⦵298)
|
93 J•mol−1•K−1[4] | ||
Standart formasyon entalpisi (ΔfH⦵298)
|
-1207 kJ•mol−1[4] | ||
| Farmakoloji | |||
| A02AC01 (DSÖ) A12AA04 (DSÖ) | |||
| Tehlikeler | |||
| NFPA 704 (yangın karosu) |
|||
| Öldürücü doz veya konsantrasyon (LD, LC): | |||
LD50 (medyan doz)
|
6450 mg/kg (oral, sıçan) | ||
| NIOSH ABD maruz kalma limitleri: | |||
| PEL (izin verilen) | TWA 15 mg/m³ (toplam) TWA 5 mg/m³ (solunum) | ||
| AB İndeksi | Listede yer almamaktadır | ||
| Güvenlik bilgi formu (SDS) | ICSC 1193 | ||
| Benzeyen bileşikler | |||
Diğer anyonlar
|
Kalsiyum bikarbonat | ||
Diğer katyonlar
|
Magnezyum karbonat Stronsiyum karbonat Baryum karbonat | ||
Benzeyen bileşikler
|
Kalsiyum sülfat | ||
| Aksi belirtilmediği sürece madde verileri, Standart sıcaklık ve basınç koşullarında belirtilir (25 °C [77 °F], 100 kPa).
| |||
| Bilgi kutusu kaynakları | |||

Kalsiyum karbonatın doğada bulunduğu kayaçlar içinde en yoğun bilinenleri, aragonit, kalsit, vaterit, tebeşir, kireç taşı, mermer ve travertendir. Bir kayaç üzerinde kalsiyum karbonatın varlığının tespit edilmesi için hidroklorik asit veya sülfürik asit kullanılır.
Kimyasal özellikleri
değiştir- Kalsiyum karbonat, diğer karbonat türleriyle hemen hemen aynı özellikleri taşır. Güçlü asitlerle karşılaştığında karbon dioksit gazı açığa çıkar:
- CaCO3(k) + 2HCl(s) → CaCl2(s) + CO2(g) + H2O(s)
- Yine 840 °C'ye kadar ısınan kalsiyum karbonat, karbon dioksit açığa çıkarır ve entalpi 178 kJ/mol enerjisiyle kalsiyum oksit ve karbon dioksit oluşur:
- CaCO3 → CaO + CO2
Kullanım alanları
değiştirKalsiyum karbonat, sanayide, mermer, tebeşir ve kireç taşı gibi farklı malzemelerin üretiminde yoğun olarak kullanılır. Aynı şekilde boya malzemelerinin üretilmesinde yoğun olarak bu bileşikten yararlanılır. PVC üretiminde de kullanılan kalsiyum karbonat, seramik yapımında yararlanılan bir moleküldür. Tıp alanında,genellikle Böbrek fonksiyonunu kaybetmiş, kandaki fosforu idrar yolu ile atamayan kronik böbrek yetersizliği durumlarında besinlerdeki fosforu bağlamasında, fosfatlı bileşiklerin dengelenmesinde kullanılır. (phos-ex) Gıda alanında ise E170 adıyla katkı maddesi şeklinde ve soya sütünde kullanılır. Son yıllarda çevresel dengenin sağlanmasında kalsiyum karbonatın önemli bir yere sahip olduğu görülmüştür.
Ayrıca bakınız
değiştirKaynakça
değiştir- ^ Aylward, Gordon and Findlay, Tristan (2008). SI Chemical Data Book (4th ed.). John Wiley & Sons Australia, Ltd. ISBN 978-0-470-81638-7.
- ^ Rohleder, J.; Kroker, E. (2001). Calcium Carbonate: From the Cretaceous Period Into the 21st Century. Springer Science & Business Media. ISBN 3-7643-6425-4. 19 Ocak 2017 tarihinde kaynağından arşivlendi. Erişim tarihi: 22 Eylül 2015.
- ^ "Occupational safety and health guideline for calcium carbonate" (PDF). US Dept. of Health and Human Services. 22 Haziran 2015 tarihinde kaynağından arşivlendi (PDF). Erişim tarihi: 31 Mart 2011.
- ^ a b Zumdahl, Steven S. (2009). Chemical Principles 6th Ed. Houghton Mifflin Company. s. A21. ISBN 0-618-94690-X.