Benzoëzuur
| Benzoëzuur | ||||
|---|---|---|---|---|
| Structuurformule en molecuulmodel | ||||
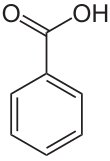
| ||||
Structuurformule van benzoëzuur
| ||||

| ||||
Benzoëzuurkristallen
| ||||
| Algemeen | ||||
| Molecuulformule | ||||
| IUPAC-naam | benzeencarbonzuur | |||
| Andere namen | carboxybenzeen | |||
| Molmassa | 122,13 g/mol | |||
| SMILES | c1ccccc1C(=O)O
| |||
| CAS-nummer | 65-85-0 | |||
| EG-nummer | 200-618-2 | |||
| Wikidata | Q191700 | |||
| Beschrijving | Wit poeder of kristallen met een naaldvormig karakter. | |||
| Waarschuwingen en veiligheidsmaatregelen | ||||
| ||||
| H-zinnen | H302 - H319 | |||
| EUH-zinnen | geen | |||
| P-zinnen | P305+P351+P338 | |||
| LD50 (ratten) | 1700 mg/kg | |||
| Fysische eigenschappen | ||||
| Aggregatietoestand | vast | |||
| Kleur | wit | |||
| Dichtheid | 1,27 g/cm³ | |||
| Smeltpunt | 122,4 °C | |||
| Kookpunt | 249 °C | |||
| Vlampunt | 121 °C | |||
| Goed oplosbaar in | chloroform, ethanol, aceton | |||
| Slecht oplosbaar in | water | |||
| Evenwichtsconstante(n) | pKz = 4.202 (H2O)[1] pKz = 11.02 (DMSO)[2] | |||
| Nutritionele eigenschappen | ||||
| E-nummer | E210 | |||
| Tenzij anders vermeld zijn standaardomstandigheden gebruikt (298,15 K of 25 °C, 1 bar). | ||||
| ||||
Benzoëzuur (IUPAC: benzeencarbonzuur) is een natuurlijk voorkomende witte, kristallijne vaste stof. Zuivere kristallen hebben een ietwat typerende geur. Benzoëzuur is een zwak carbonzuur.
De stof wordt gebruikt als additief in voeding en wordt dan vaak aangeduid als E210.
De stof is genoemd naar benzoë, een hars die wordt gewonnen uit bepaalde boomsoorten van het geslacht Styrax. Benzoë bevat veel benzoëzuur en was vroeger de belangrijkste bron om deze stof te verkrijgen voor industriële toepassingen.
Benzoëzuur is verder in hoge concentratie aanwezig in cranberry's, maar komt ook voor in andere planten, met name in bessen. Vanwege zijn anti-microbiële werking, wordt het veel gebruikt als conserveermiddel in levensmiddelen en cosmetica. Ook wordt het in de land- en tuinbouw, alsmede de veehouderij gebruikt als desinfectiemiddel.
Bij een pH boven de 4,5 is benzoëzuur amper werkzaam, omdat het dan vrijwel volledig gedeprotoneerd is.
Synthese
[bewerken | brontekst bewerken]Hoewel de stof in het laboratorium meestal ook in redelijke hoeveelheden voor relatief weinig geld commercieel te verkrijgen is, kan de stof ook via een groot aantal syntheseroutes bereid worden. De ene methode is wat goedkoper dan de andere. Meestal wordt het verkregen door tolueen te oxideren met een oxidator zoals kaliumdichromaat, kaliumchromaat of kaliumpermanganaat. De reagentia worden in water gedurende een aantal uur gerefluxt. Er ontstaat het kaliumzout. Het zuur wordt gewonnen door toevoegen van een verdunde zoutzuuroplossing. De stof laat zich vrij gemakkelijk omkristalliseren uit water.
De industriële bereiding wordt ook gedaan op grote schaal door oxidatie van tolueen. Hier echter kiest men vanuit een financieel oogpunt vaak voor het gebruik van lucht-zuurstof en een katalysator (meestal ijzer).
Benzoëzuur als conserveermiddel
[bewerken | brontekst bewerken]Benzoëzuur wordt onder andere aan levensmiddelen toegevoegd als conserveermiddel en is bekend onder het E-nummer E210. De INCI-code is Benzoic acid. Ook verschillende zouten van benzoëzuur worden als zodanig toegepast als E211-E213.
Benzoëzuur is als conserveermiddel echter omstreden, omdat het onder bepaalde omstandigheden in combinatie met ascorbinezuur (vitamine C) alsmede koper- of ijzer-zouten voor een heel klein deel kan worden omgezet in het giftige benzeen. Of het de ophef waard is, is weer een andere vraag. Sommige onderzoekers trekken namelijk in twijfel dat die kleine hoeveelheden ook daadwerkelijk een bijdrage leveren aan de totale benzeenblootstelling.[3]
Er is een relevante groep mensen allergisch voor benzoaat-verbindingen die in cremes en cosmetica worden toegepast. Het wordt ook toegepast als conserveermiddel van verdovingsvloeistof van tandartsen. Artsen van de pijnpoli verzamelen hier informatie over. Alternatieven zijn voorhanden, door verdovingsstof zonder conserveermiddel bij deze groep mensen te gebruiken.
Anti-schimmelwerking
[bewerken | brontekst bewerken]In de geneeskunde wordt benzoëzuur toegepast als middel tegen huidschimmels. Een bekend middel is Whitfield-zalf, een zalf die als werkende bestanddelen benzoëzuur en salicylzuur bevat.[4]
Toepassing
[bewerken | brontekst bewerken]'s Werelds grootste producent van benzoëzuur en afgeleide producten is Emerald Kalama Chemical (vroeger DSM Special Products) in Rozenburg. Zij leveren het onder meer onder de merknaam VevoVitall als additief (zuurteregelaar) aan diervoeder, meer bepaald varkensvoer. Het zorgt er volgens DSM voor dat de ammoniakemissie naar de lucht met 30% vermindert.[5] De Europese Commissie heeft dit gebruik van benzoëzuur in varkensvoer op 21 mei 2003 voorlopig toegestaan. Op 29 juni 2007 is door de EC een permanente autorisatie verleend, onder Commission Regulation (EC) No 757/2007.
Zie ook
[bewerken | brontekst bewerken]Externe links
[bewerken | brontekst bewerken]- ↑ Harris, Daniel (2010). Quantitative Chemical Analysis, 8. W. H. Freeman and Company, New York, AP12. ISBN 9781429254366.
- ↑ Olmstead, William N., Bordwell, Frederick G. (1980). Ion-pair association constants in dimethyl sulfoxide. The Journal of Organic Chemistry 45 (16): 3299–3305. DOI: 10.1021/jo01304a033.
- ↑ Indications of the possible formation of benzene from benzoic acid in foods BfR Expert Opinion No. 013/2006, 1 December 2005. Gearchiveerd op 19 juli 2011.
- ↑ http://www.apotheek.net/Medische_informatie/Medicijnen/Producten/Whitfield_s_zalf_of_cr_me.aspx?mId=10704&rId=794[dode link]
- ↑ (en) DSM informatiepagina over VeoVitall


