Oxyde de sodium
Apparence
| Oxyde de sodium | |
| |
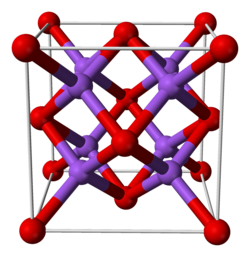
| Structure cristalline de l'oxyde de sodium. | |
| Identification | |
|---|---|
| Nom UICPA | Oxyde de sodium |
| No CAS | |
| No ECHA | 100.013.827 |
| No CE | 215-208-9 |
| SMILES | |
| InChI | |
| Apparence | solide blanc |
| Propriétés chimiques | |
| Formule | Na2O [Isomères] |
| Masse molaire[1] | 61,978 9 ± 0,000 3 g/mol Na 74,19 %, O 25,81 %, |
| Propriétés physiques | |
| T° fusion | 1 132 °C[réf. souhaitée] |
| T° ébullition | 1 950 °C[réf. souhaitée] |
| Cristallographie | |
| Système cristallin | Cubique |
| Symbole de Pearson | [2] |
| Classe cristalline ou groupe d’espace | Fm3m (no 225)[2] |
| Strukturbericht | C1[2] |
| Structure type | CaF2[2] |
| Précautions | |
| SIMDUT[3] | |
 E, |
|
| Directive 67/548/EEC | |
| Composés apparentés | |
| Autres cations | Oxyde de lithium Oxyde de potassium Oxyde de césium Oxyde de rubidium |
| Autres anions | Hydroxyde de sodium Sulfure de sodium Tellurure de sodium |
| Autres composés | |
| Unités du SI et CNTP, sauf indication contraire. | |
| modifier |
|
L'oxyde de sodium est un composé chimique de formule Na2O. Cet oxyde réagit avec l'eau pour donner de l'hydroxyde de sodium. Il est utilisé dans la fabrication du verre en tant que fondant.
Références
[modifier | modifier le code]- Masse molaire calculée d’après « Atomic weights of the elements 2007 », sur www.chem.qmul.ac.uk.
- « The Fluorite (C1) Structure », sur cst-www.nrl.navy.mil (consulté le ).
- « Oxyde de sodium » dans la base de données de produits chimiques Reptox de la CSST (organisme québécois responsable de la sécurité et de la santé au travail), consulté le 25 avril 2009.


