ثلاثي ميثيل الألومنيوم
مركب كيميائي
ثلاثي ميثيل الألومنيوم هو مركب ألومنيوم عضوي صيغته C6H18Al2، كما يكتب على الشكل التالي Al2(CH3)6، ويوجد على شكل سائل عديم اللون.
| ثلاثي ميثيل الألومنيوم | |
|---|---|
| الاسم النظامي (IUPAC) | |
Trimethylalumane |
|
| أسماء أخرى | |
Trimethylaluminum; aluminium trimethyl; aluminum trimethyl |
|
| المعرفات | |
| الاختصارات | TMA |
| CAS | 75-24-1 |
| بوب كيم | 16682925[1] |
مواصفات الإدخال النصي المبسط للجزيئات
|
|
| الخواص | |
| الصيغة الجزيئية | C6H18Al2 |
| الكتلة المولية | 144.18 غ/مول (ديمر) |
| المظهر | سائل عديم اللون |
| الكثافة | 0.75 غ/سم3 |
| نقطة الانصهار | 15 °س |
| نقطة الغليان | 125 °س |
| الذوبانية في الماء | يتفاعل |
| المخاطر | |
| رمز الخطر وفق GHS |   |
| وصف الخطر وفق GHS | خطر |
| في حال عدم ورود غير ذلك فإن البيانات الواردة أعلاه معطاة بالحالة القياسية (عند 25 °س و 100 كيلوباسكال) | |
| تعديل مصدري - تعديل | |
التحضير
عدليحضر المركب من تفاعل الألومنيوم مع كلورو الميثان بوجود الصوديوم:
الخواص
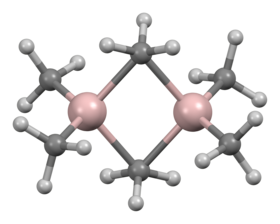
عدليوجد المركب في الشروط القياسية على شكل سائل عديم اللون، وهو يتفاعل بعنف عند التماس مع الماء. يتألف المركب من بنية ثنائية الوحدات على الشكل Al2R6، حيث تمثل R مجموعة الميثيل؛ ويكون مركز الألومنيوم على شكل رباعي وجوه.[2] ترتبط ذرتا الكربون ببعض بربيطة جسرية؛ ويختلف طول الرابطة Al-C عندما تكون طرفية (1.97 أنغستروم) عنها عندما تكون جسرية (2.14 أنغستروم).
يتفكك المركب إلى المونومير (أحادي القسيمة) AlMe3 عند التسخين.[3]
الاستخدامات
عدلللمركب عدد من التطبيقات في مجال الاصطناع العضوي.
طالع أيضاً
عدلالمراجع
عدل- ^ ا ب ج د Trimethylaluminum (بالإنجليزية), QID:Q278487
- ^ Holleman, A. F.؛ Wiberg, E. (2001). Inorganic Chemistry. San Diego: Academic Press. ISBN:0-12-352651-5.
- ^ Vass، Gábor؛ Tarczay، György؛ Magyarfalvi، Gábor؛ Bödi، András؛ Szepes، László (2002). "HeI Photoelectron Spectroscopy of Trialkylaluminum and Dialkylaluminum Hydride Compounds and Their Oligomers". Organometallics. ج. 21 ع. 13: 2751–2757. DOI:10.1021/om010994h.
في كومنز صور وملفات عن Trimethylaluminium.